
分析 (1)燃烧热是指在25摄氏度,101 kPa时,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量为1mol,产物必须是稳定氧化物据此解答;
(2)依据氢气燃烧的热化学方程式计算;
(3)根据盖斯定律,将反应③④做相应的变形即可.
解答 解:(1)根据燃烧热的定义,1mol氢气燃烧生成液态水更稳定,所以①H2(g)+$\frac{1}{2}$O2(g)=H2O(l);△H=-285kJ•mol-1为氢气燃烧热的化学方程式,所以氢气的燃烧热为:285kJ•mol-1;根据燃烧热的定义,1mol碳完全燃烧生成二氧化碳时放出的热量为碳的燃烧热,④C(s)+O2 (g)=CO2(g);△H=-393.5kJ•mol-1为碳燃烧热的化学方程式,所以碳的燃烧热为:393.5kJ•mol-1;
故答案为:285kJ•mol-1;393.5kJ•mol-1;
(2)H2(g)+$\frac{1}{2}$O2(g)=H2O (l) Q
2g 285kJ
10g 1425KJ
所以燃烧10gH2生成液态水,放出的热量为1425KJ,
故答案为:1425KJ;
(3)由于CO的燃烧热的化学方程式为CO(g)+$\frac{1}{2}$O2(g)═CO2(g),根据盖斯定律,将④-③即可得:CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-393.5kJ/mol-(-241.8kJ/mol)=-151.7KJ/mol,故答案为:CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-151.7KJ/mol,
点评 本题考查了燃烧热的定义和反应热的求算,题目难度不大,理解燃烧热概念时注意:1、物质的物质的量必须是1mol;2、必须是完全燃烧生成稳定的氧化物.


科目:高中化学 来源: 题型:解答题
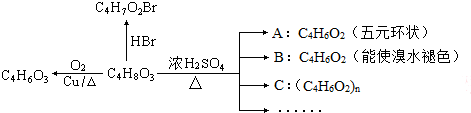
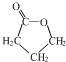 +H2O;
+H2O; .合成路线示例如下:
.合成路线示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都可以与溴发生取代反应 | |
| B. | 乙烯易发生加成反应,苯不能发生加成反应 | |
| C. | 常温下都是气态物质 | |
| D. | 乙烯易被酸性高锰酸钾溶液氧化,而苯不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
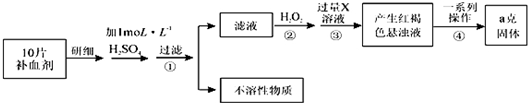

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图是A分子的球棍模型和B分子的比例模型,回答下列问题:
如图是A分子的球棍模型和B分子的比例模型,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个反应都是置换反应 | B. | 反应①是放热反应 | ||
| C. | 上述两个反应是可逆反应 | D. | 两个反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
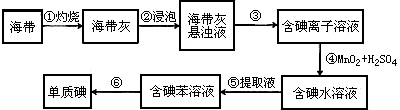
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③④ | C. | ②④ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com