
科目:高中化学 来源:不详 题型:单选题
| A.N2与O2反应生成NO |
| B.NH3经催化氧化生成NO |
| C.N2和H2在一定条件下合成氨 |
| D.豆科植物的根瘤菌将空气中的氮气转化为含氮化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.7毫升 | B.8毫升 | C.11毫 | D.13毫升 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
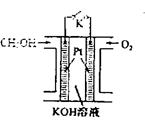
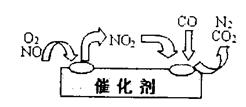
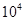 L(标准状况)该尾气需42.5gNH3,则x= 。
L(标准状况)该尾气需42.5gNH3,则x= 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨工业中将氮气与氢气化合生成氨气 |
| B.N2和O2经放电生成NO |
| C.通过加压、降温等方法将氮气转变为液态氮 |
| D.NH3被H2SO4硫酸吸收生成(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在AsCl3分子中,砷原子最外层电子数为8; |
| B.Na3AsO4溶液的pH大于7; |
| C.砷的氢化物的化学式为AsH3,它的沸点比NH3低; |
| D.砷的相对原子质量为74.92,由此可知砷原子核内有42个中子。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com