
沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O时,放出
445 kJ的热量,则表示CH4燃烧热的热化学方程式正确的是
A.1/2CH4(g)+O2(g)= 1/2CO2(g)+H2O (l) ΔH =-445 kJ/mol
B.CH4+2O2=CO2+H2O ΔH=-890 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2 H2O (l) ΔH =-890 kJ/mol
D.CH4(g)+2O2(g)=CO2(g)+2H2O (l) ΔH = +890 kJ/mol
科目:高中化学 来源:2016届宁夏银川二中高三5月适应性训练理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.生活中常用热的小苏打去污,利用了水解吸热的特点
B.Mg可由电解MgCl2水溶液制取,Al可由电解熔融Al2O3制取
C.少数商贩在蔬菜表面洒少许福尔马林,可延长保鲜时间
D.SiO2可用来制作光导纤维,但SiO2本身不导电
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三高考前模拟理综化学试卷(解析版) 题型:选择题
某试液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如下实验:
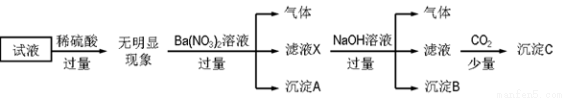
下列说法正确的是( )
A.无法确定原试液中是否含有Al3+、Cl-
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.无法确定沉淀C的成分
D.原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市高三高考前最后一卷理综化学试卷(解析版) 题型:选择题
某有机物M 7.4 g与足量氧气反应后,所得气体依次通过盛有浓H2SO4和碱石灰的装置,两装置分别增重9 g和17.6 g;同温同压下,M蒸汽的密度是H2的37倍,则能够与钠反应放出H2的M的同分异构体的数目(不考虑立体异构)
A.8 B.6 C.4 D.2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下第二次段考化学卷(解析版) 题型:选择题
可逆反应2NO2 ? 2NO + O2在恒容密闭容器中进行,可以作为达到平衡状态的标志是
A.NO2的反应速率与NO的反应速率相等
B.混合气体的颜色不再改变
C.混合气体的密度不再改变的状态
D.单位时间内生成n molO2的同时生成2nmolNO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下第二次段考化学卷(解析版) 题型:选择题
下列物质中酸性最强的是
A. H2SiO3 B.H3PO4 C.H2SO4 D.HClO4
H2SiO3 B.H3PO4 C.H2SO4 D.HClO4
查看答案和解析>>
科目:高中化学 来源:2016届江苏省等三校高三第四次模拟化学试卷(解析版) 题型:填空题
有机物G是一种重要的有机合成中间体,可通过以下方法合成:
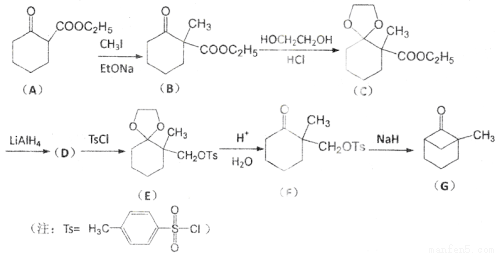
(1)写出A中含氧官能团的名称:____________和____________。
(2)写出D的结构简式:____________;
(3)将B转化为化合物C的反应目的是____________;
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式:____________;
①能发生水解反应
②能使溴的CC14溶液褪色
③分子中有2种不同化学环境的氢原子
(5)根据己有知识并结合相关信息写出以丁烯酮(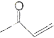 )、乙醛、乙二醇为主要原料制备5-羟基-2-己酮(
)、乙醛、乙二醇为主要原料制备5-羟基-2-己酮(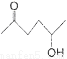 )的合成路线流程图(有机溶剂乙醚和无机试剂任用)。合成路线流程图示例如下:
)的合成路线流程图(有机溶剂乙醚和无机试剂任用)。合成路线流程图示例如下:
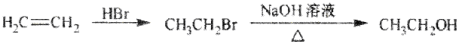
己知:卤代烃可以和Mg生成格氏试剂(RMgX ),醛或酮可以和格氏试剂反应:
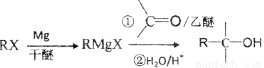
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月模拟四理综化学试卷(解析版) 题型:推断题
G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线如下(部分产物和部分反应条件略去):
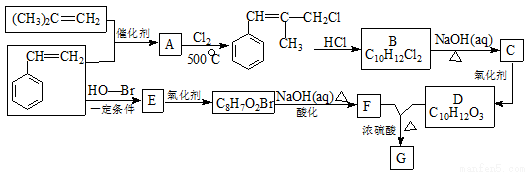
已知:①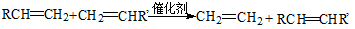 ;
;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子;
③D和F是同系物。
请回答下列问题:
(1)(CH3)2C=CH2的系统命名法名称为 。
(2)A→B反应过程中涉及的反应类型依次为 、 。
(3)D分子中含有的含氧官能团名称是 ,G的结构简式为 。
(4)生成E的化学方程式为 。
(5)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基、含C=O的F的同分异构体有 种(不包括立体异构);其中核磁共振氢谱为4组峰、能水解的所有物质的结构简式为 。
(6)模仿由苯乙烯合成F的方法,写出由丙烯制取α-羟基丙酸(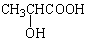 )的合成线路: 。
)的合成线路: 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:填空题
磷元素的含氧酸有磷酸、亚磷酸、次磷酸等很多种,其中亚磷酸(H3PO3)是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
(1)写出亚磷酸与足量NaOH溶液反应的离子方程式____________________________;
(2)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为______________;
(3)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的电离平衡常数K=___________________;(H3PO3第二步电离忽略不计,结果保留两们有效数字)
(4)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)_____c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”,下同);在NaH2PO3溶液中,c(H+)+c(H3PO3)_____c(HPO32-)+c(OH-)
(5)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:
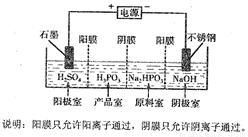
①产品室中反应的离子方程式为_______________________;
②得到1mol亚磷酸的同时,阴极室制得NaOH质量为________g。
(6)已知铵盐的分解比较复杂,但分解时不涉及到化合价变化的铵盐分解比较简单,其实质就是质子的转移(如NH4A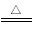 NH3+HA),磷酸对应的各种铵盐分解时不涉及化合价变化,试从酸根离子结合氢离子难易的解度,判断下列铵盐的分解温度:
NH3+HA),磷酸对应的各种铵盐分解时不涉及化合价变化,试从酸根离子结合氢离子难易的解度,判断下列铵盐的分解温度:
NH4H2PO4____________(NH4)2HPO4(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com