
【题目】KClO3是一种常见的氧化剂,常用于医药工业、印染工业和制造烟火.实验室用KClO3和MnO2混合加热制氧气,现取KClO3和MnO2混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g(25℃),再加5g水充分溶解,仍剩余固体4.80g(25℃).
(1)若剩余的4.80g固体全是MnO2 , 则原混合物中KClO3的质量为g;
(2)若剩余的4.80g固体是MnO2和KCl的混合物
(a)求25℃时KCl的溶解度;
(b)求原混合物中KClO3的质量;
(c)所得KCl溶液的密度为1.72g/cm3 , 则溶液的物质的量浓度为多少?(保留2位小数)
【答案】
(1)11.80
(2)35g,12.25g,5.99mol/L
【解析】解:(1)若剩余的4.80g固体全是MnO2,m(KClO3)=16.60g﹣4.80g=11.80g,
所以答案是:11.80;(2)若剩余的4.80g固体是MnO2和KCl的混合物,则5g水溶解氯化钾得到的溶液是饱和溶液,5g水溶解KCl的质量=6.55g﹣4.80g=1.75g,
(a)则100g水溶解KCl的质量= ![]() ×100g=35g,答:25℃时KCl的溶解度35g;
×100g=35g,答:25℃时KCl的溶解度35g;
(b)20g水溶解氯化钾的质量=1.75g×4=7g,反应前后质量减少的质量为氧气的质量,氧气的质量=16.60g﹣7g﹣4.80g=4.8g,根据氧原子守恒得 ![]() ×122.5g/mol=12.25,答:原混合物中KClO3的质量12.25g;
×122.5g/mol=12.25,答:原混合物中KClO3的质量12.25g;
(c)溶液的质量=20g+7g=27g,溶液的体积= ![]() ,n(KCl)=
,n(KCl)= ![]() ,则溶液的物质的量浓度=
,则溶液的物质的量浓度= ![]() =5.99mol/L,
=5.99mol/L,
答:溶液的物质的量浓度为5.99mol/L.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生。则下列结论正确的是
A. 滤液中一定有Fe(NO3)3
B. 滤渣只含Ag和Cu,一定无Zn
C. 滤渣中一定有Ag、Cu和Fe,一定无Zn
D. 滤渣中一定有Ag、Cu、Fe和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿的主要成分是CuFeS2(硫元素﹣2价,铁元素+2价).实验室用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如图: 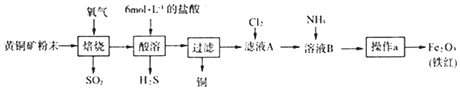
已知:CuFeS2+O2 ![]() Cu+FeS+SO2 FeS+2HCl=FeCl2+H2S↑
Cu+FeS+SO2 FeS+2HCl=FeCl2+H2S↑
(1)实验室制氯气的化学方程式为 .
(2)SO2和H2S有毒,会造成大气污染.
①已知SO2和H2S混合可以得到单质硫.为使SO2和H2S恰好完全转化为硫,二者体积(标准状况)比应为 .
为检验某尾气中是否含有SO2、CO2、CO三种气体,实验小组同学用如下装置设计实验.
选择上述装置(可以重复),按照气流方向其连接顺序为A→(填序号).
(3)PbO2具有强氧化性,可与浓盐酸反应制取氯气.
①上述反应化学方程式为;由PbO与次氯酸钠溶液反应可制得PbO2 , 反应的离子方程式为 .
②Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”.Na2S2O3在溶液中被Cl2氧化成SO42﹣ , 则该反应的化学方程式为 .
③本实验存在的一个缺陷是 .
(4)按上述流程用150g黄铜矿粉末可制得48gFe2O3(铁红),则该黄铜矿中含CuFeS2的质量分数是(假设各步反应均完全进行且过程中无额外物质损耗).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是在实验室进行二氧化硫制备与验证性质实验的组合装置,部分固定装置未画出. 
(1)装置B中试剂X是 , 装置D中盛放NaOH溶液的作用是 .
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是 .
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I﹣还原性弱于SO2的现象为;发生反应的离子方程式是 .
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验: 取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应.上述方案是否合理?(填“合理”或“不合理”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同学小明上完氯气性质一节仍感意犹未尽,自己又在老师的指导下做了氯气与金属铝的反应,实验前老师要求他查一下氯化铝的相关理化数据,他发现氯化铝的熔点为190℃(2.02×105 Pa),而沸点是180℃
(1)常压下持续加热AlCl3 , AlCl3会(填物理变化过程)
(2)根据这些数据,可以推测氧化铝是晶体,可进一步验证这个结论的是: . A.熔融氯化铝不导电 B.氯化铝溶液可导电
C.氯化铝温室下为固体 D.氢氧化铝溶于盐酸可生成氯化铝
(3)又查得,氯化铝蒸气的密度(换算成标准状况时)为11.92gL﹣1 , 氯化铝的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(1)分子式的确定: (i)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2 , 消耗氧气6.72L(标准状况下),则该物质中各元素的原子个数比是 .
(ii)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为 , 该物质的分子式是 .
(ii)根据价键理论,预测A的可能结构并写出结构简式 .
(2)结构式的确定: 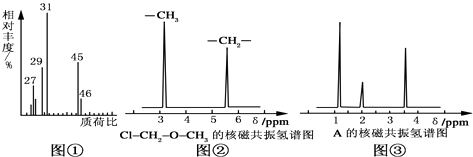
(i)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl2﹣CH2﹣O﹣CH3)有两种氢原子如图②.经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为 .
(ii)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式: .
(iii)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图1所示装置进行实验,请回答下列问题: 
(1)若开始实验时开关K与a连接,则B极的电极反应式为 .
(2)若开始实验时开关K与b连接,则下列说法正确的是(填序号). ①溶液中Na+向A极移动
②从A极逸出的气体能使湿润的淀粉KI试纸变蓝
③反应一段时间后向电解液中加适量盐酸可恢复到电解前的浓度
(3)该小组运用工业上离子交换膜法制烧碱的原理,用如图2所示装置电解K2SO4溶液. ①该电解槽的阳极反应式为 , 通过阴离子交换膜的离子数(填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为;
③电解一段时间后,B口与C口产生气体的质量比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 元素周期表中元素排序的依据是元素的相对原子质量
B. 阴、阳离子通过静电引力形成离子键
C. 元素周期表有十八个纵行,也就是十六个族
D. 只有在活泼金属元素和活泼非金属元素化合时,才能形成离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com