
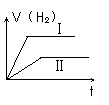
实验Ⅰ和实验Ⅱ均为Zn与盐酸反应,若实验Ⅰ用锌粉,实验Ⅱ用锌粒,且两实验用锌量相同,加入的盐酸也是等浓度、等体积的,则两实验产生的H2的量与时间的关系如下图所示,正确的是 ( )
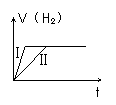 | |||||||
 | |||||||
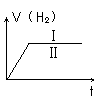 |  | ||||||
A B C D
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解



| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:解答题
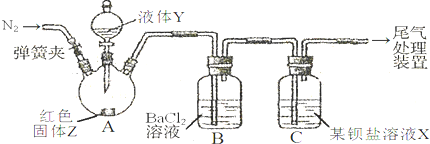
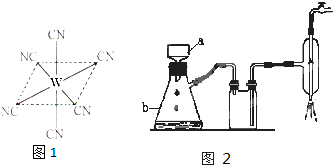
| 操 作 | 现 象 |
| 关闭弹簧夹,滴加一定量液体Y,加强热; | A中有白雾生成,红色固体Z的表面产生气泡.B中有气泡冒出,产生大量白色沉淀.C中产生白色沉淀,液面上方略显红棕色并逐渐消失. |
| 打开弹簧夹,通入气体N2,停止加热,一段时间后关闭; | |
| 从B、C中分别取少量白色沉淀,加稀盐酸. | 均未发现白色沉淀溶解 |
| 甲 | 大量不溶于稀盐酸的白色沉定 |
| 乙 | 少量不溶于稀盐酸的白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com