½ā“š£ŗ½ā£ŗ£Ø1£©ÓÉH
2£Øg£©µÄČ¼ÉÕČČ”÷HĪŖ-285.8kJ?mol
-1ÖŖ£¬1molH
2£Øg£©ĶźČ«Č¼ÉÕÉś³É1molH
2O£Øl£©·Å³öČČĮæ285.8kJ£¬
¼“·Ö½ā1mol H
2O£Øl£©ĪŖ1mol H
2£Øg£©ĻūŗĵÄÄÜĮæĪŖ285.8kJ£¬Ōņ·Ö½ā5mol H
2O£Øl£©ĻūŗĵÄÄÜĮæĪŖ285.8kJ”Į5=1429kJ£¬
¹Ź“š°øĪŖ£ŗ1429£»
£Ø2£©ÓÉCO£Øg£©ŗĶCH
3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-283.0kJ?mol
-1ŗĶ-726.5kJ?mol
-1£¬Ōņ
¢ŁCO£Øg£©+
O
2£Øg£©=CO
2£Øg£©”÷H=-283.0kJ?mol
-1 ¢ŚCH
3OH£Øl£©+
O
2£Øg£©=CO
2£Øg£©+2 H
2O£Øl£©”÷H=-726.5kJ?mol
-1 ÓÉøĒĖ¹¶ØĀÉæÉÖŖ£¬¢Ś-¢ŁµĆ·“Ó¦CH
3OH£Øl£©+O
2£Øg£©=CO£Øg£©+2 H
2O£Øl£©£¬Ōņ”÷H=-726.5kJ?mol
-1-£Ø-283.0kJ?mol
-1£©=-443.5kJ?mol
-1£¬
¹Ź“š°øĪŖ£ŗCH
3OH£Øl£©+O
2£Øg£©=CO£Øg£©+2 H
2O£Øl£©”÷H=-443.5kJ?mol
-1£»
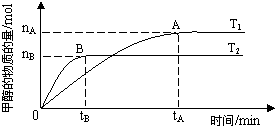
£Ø3£©øł¾ŻĢāøųĶ¼Ļó·ÖĪöæÉÖŖ£¬T
2ĻČ“ļµ½Ę½ŗāŌņT
2£¾T
1£¬ÓÉĪĀ¶ČÉżøß·“Ó¦ĖŁĀŹŌö“óæÉÖŖT
2µÄ·“Ó¦ĖŁĀŹ“óÓŚT
1£¬ÓÖĪĀ¶Čøߏ±Ę½ŗāדĢ¬CH
3OHµÄĪļÖŹµÄĮæÉŁ£¬ŌņĖµĆ÷æÉÄę·“Ó¦CO
2+3H
2?CH
3OH+H
2OĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬¹ŹÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ŌņT
1Ź±µÄĘ½ŗā³£Źż±ČT
2Ź±µÄ“ó£»
¢Łv£ØCH
3OH£©=
=
mol/L?min£¬¹Ź¢Ł“ķĪó£»
¢ŚŅĄ¾ŻĶ¼Ļó·ÖĪöT
2ĻČ“ļµ½Ę½ŗāŌņT
2£¾T
1£¬ÓÉĪĀ¶ČÉżøß·“Ó¦ĖŁĀŹŌö“óæÉÖŖT
2µÄ·“Ó¦ĖŁĀŹ“óÓŚT
1£¬ÓÖĪĀ¶Čøߏ±Ę½ŗāדĢ¬CH
3OHµÄĪļÖŹµÄĮæÉŁ£¬ŌņĖµĆ÷æÉÄę·“Ó¦CO
2+3H
2?CH
3OH+H
2OĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬¹ŹÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¹Ź¢ŚÕżČ·£»
¢ŪÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øł¾ŻĢāøųĶ¼Ļó·ÖĪöæÉÖŖ£¬T
2ĻČ“ļµ½Ę½ŗāŌņT
2£¾T
1£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬øĆ·“Ó¦ŌŚT
1Ź±µÄĘ½ŗā³£Źż±ČT
2Ź±µÄ“󣬹Ź¢Ū“ķĪó£»
¢Ü“¦ÓŚAµćµÄ·“Ó¦ĢåĻµ“ÓT
1±äµ½T
2£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬“ļµ½Ę½ŗāŹ±£¬ĒāĘųĪļÖŹµÄĮæŌö“󔢼ד¼µÄĪļÖŹµÄĮæ¼õŠ”£¬¹Ź
Ōö“󣬹Ź¢ÜÕżČ·£»
¹Ź“š°øĪŖ£ŗ¢Ś¢Ü£»
£Ø4£©ÓÉ»ÆŃ§Ę½ŗāµÄČż¶ĪÄ£Ź½·Ø¼ĘĖćæÉÖŖ£¬
CO
2 £Øg£©+3H
2£Øg£©=CH
3OH£Øg£©+H
2O£Øg£©
ĘšŹ¼ 1 3 0 0
񄯒 a 3a a a
Ę½ŗā 1-a 3-3a a a
øł¾ŻĻąĶ¬Ģõ¼žĻĀĘųĢåµÄŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬
ŌņČŻĘ÷ÄŚµÄŃ¹ĒæÓėĘšŹ¼Ń¹ĒæÖ®±ČĪŖ=£Ø1-a+3-3a+a+a£©£ŗ£Ø1+3£©=£Ø2-a£©£ŗ2£¬
¹Ź“š°øĪŖ£ŗ£Ø2-a£©£ŗ2£®

 æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®
æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®

 ¶į¹ŚŃµĮ·µ„ŌŖĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
¶į¹ŚŃµĮ·µ„ŌŖĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø ŠĀĖ¼Ī¬Š”¹Ś¾ü100·Ö×÷Ņµ±¾ĻµĮŠ“š°ø
ŠĀĖ¼Ī¬Š”¹Ś¾ü100·Ö×÷Ņµ±¾ĻµĮŠ“š°ø ĆūŹ¦Öøµ¼Ņ»¾ķĶØĻµĮŠ“š°ø
ĆūŹ¦Öøµ¼Ņ»¾ķĶØĻµĮŠ“š°ø
 £Ø2011?½Ī÷£©æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø2011?½Ī÷£©æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®
æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£® æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£®
æĘѧ¼ŅĄūÓĆĢ«ŃōÄÜ·Ö½āĖ®Éś³ÉµÄĒāĘųŌŚ“߻ƼĮ×÷ÓĆĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³É¼×“¼£¬²¢æŖ·¢³öÖ±½ÓŅŌ¼×“¼ĪŖČ¼ĮĻµÄČ¼ĮĻµē³Ų£®ŅŃÖŖH2£Øg£©”¢CO£Øg£©ŗĶCH3OH£Øl£©µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-285.8kJ?mol-1”¢-283.0kJ?mol-1ŗĶ-726.5kJ?mol-1£® Ģ¼ŹĒ»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£¬Ę䵄֏¼°»ÆŗĻĪļŹĒČĖĄąÉś²śÉś»īµÄÖ÷ŅŖÄÜŌ“ĪļÖŹ£®
Ģ¼ŹĒ»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£¬Ę䵄֏¼°»ÆŗĻĪļŹĒČĖĄąÉś²śÉś»īµÄÖ÷ŅŖÄÜŌ“ĪļÖŹ£®