
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体。A、B、C、D、E、F和OPA的转化关系如下所示:

回答下列问题:
(1)A的化学名称是 ;
(2)由A生成B 的反应类型是 。在该反应的副产物中,与B互为同分异构体的化合物的结构简式为 ;
(3)写出C所有可能的结构简式 ;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用化学方程式表示合成路线 ;
(5)OPA的化学名称是 ,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为 ,该反应的化学方程式为 。(提示![]() )
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式
【答案】
(1)邻二甲苯(1分)
(2)取代反应(1分) 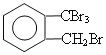 (1分)
(1分)
(3) (2分)
(2分)
(4) (2分)
(2分)
(5)邻苯二甲醛(1分) 缩聚反应(1分)
 (2分)
(2分)
(6)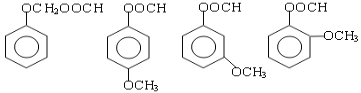 (4分)
(4分)
【解析】
(1)由合成路线图知:芳香化合物A分子式为C8H10,且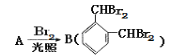 可推知A为邻二甲苯;
可推知A为邻二甲苯;
(2)A→B的反应类型是取代反应,因取代反应是连锁反应,有多种副产物。 所以与B互为同分异构体的化合物的结构简式为:
(3)A→C(C8H9Br),条件是Br2/FeBr3,可知发生的是苯环上的取代,又因甲基是邻、对位定位基,则C的可能结构简式有两种分别是:
(4)D为邻苯二甲酸二乙酯,A→D经两步合成,可先用酸性K2MnO4将邻二甲苯氧化为邻苯二甲酸;然后再与乙醇发生酯化反应制得。
(5)由OPA的结构简式知其名称为邻苯二甲醛,易错命名为邻二苯甲醛,注意命名时应以官能团醛基为母体。OPA→E(C8H8O3),结合题给信息可知:在此条件下—CHO即可被氧化为—COOH又能被还原为—CH2OH,所以中间体E的结构简式为:![]() ;该有机物因有—COOH和—OH两种官能团,则可发生缩聚反应合成一种聚酯类高分子F,其反应为:
;该有机物因有—COOH和—OH两种官能团,则可发生缩聚反应合成一种聚酯类高分子F,其反应为: 。
。
(6)芳香化合物G是E的同分异构体,分析E的侧链可知:不饱和度=1,C原子数=2,O原子数=3,又由题干信息知其分子中含有—CHO、—COO—和—O—三种含氧官能团,综合分析得:若含一个支链则为:—OCH2OOCH;若含两个支链则分别为—OCH3和—OOCH;且它们在苯环上的位置有邻、间、对三种,所以符合条件的G的同分异构体共有4种。


科目:高中化学 来源: 题型:
【题目】某浓度的氨水中存在下列平衡:NH3·H2O![]() NH+OH-,如想增大NH的浓度,而不增大OH-的浓度,应采取的措施是
NH+OH-,如想增大NH的浓度,而不增大OH-的浓度,应采取的措施是
①适当升高温度 ②加入NH4Cl固体 ③通入NH3 ④加入少量盐酸
A. ①② B. ②③ C. ①④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出将我国建设成为制造强国,2020年我国“PX”产能将达到3496万吨/年。有机物(烃)“PX”的结构模型如下图,下列说法错误的是

A. “PX”的二氯代物共有6种(不考虑立体异构) B. “PX”的分子式为C8H10
C. “PX”分子中,最多有14个原子共面 D. 可用酸性KMnO4溶液鉴别“PX”与苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用化学用语表示9个质子,10个中子的核素:___。
(2)写出下列反应方程式
①足量的NaOH溶液与SO2反应___。
②用氯气制备漂白粉的反应____。
(3)下列物质能导电的是___,属于电解质的是___,属于非电解质的是___(填序号)。
①NaCl溶液 ②干冰 ③液态氢化氢 ④铁 ⑤硫酸钡固体 ⑥蔗糖(C12H22O11) ⑦氨气 ⑧硫酸氢钠固体
写出⑧在水溶液中的电离方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol·L-1,则该温度下水的离子积常数KW=_______mol2L-2;该温度下,pH=2的H2SO4溶液中由水电离出的[H+]为_________ molL-1。
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl ②NaOH ③H2SO4 ④(NH4)2SO4,其中水的电离程度由大到小顺序为__________________(用序号回答)。
(3)25℃时,将 a mol·L-1 的醋酸和 b mol·L-1 的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=______ molL-1,a____ b(填“﹥”、“﹤”或“=”)。
(4)常温下,稀释0.5 mol·L1的醋酸溶液,下图中的纵坐标不能表示_________

A.CH3COOH的电离程度 B.溶液中H+的数目
C.溶液中![]() 的值 D.溶液中CH3COOH的浓度
的值 D.溶液中CH3COOH的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电致变色玻璃以其优异的性能将成为市场的新宠。如图所示为五层膜的玻璃电致变色系统,其工作原理是:在外接电源下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。(已知:WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)下列有关说法正确的是

A. 当B外接电源负极时,膜由无色变为蓝色
B. 当B外接电源负极时,离子储存层发生反应为:Fe4[Fe(CN)6]3+4Li++4eˉ=Li4Fe4[Fe(CN)6]3
C. 当A接电源的负极时,此时Li+得到电子被还原
D. 当A接电源正极时,膜的透射率降低,可以有效阻挡阳光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据热化学方程式N2(g)+3H2(g)![]() 2NH3(g)+92kJ,下列有关图像和叙述中正确的是
2NH3(g)+92kJ,下列有关图像和叙述中正确的是
A.  B.
B. 
C. 向密闭容器中通入1mol氮气和3mol氢气发生反应放出92kJ的热量D. 形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量多92kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当电解质中某离子的浓度越大时,其氧化性或还原性越强,利用这一性质,有人设计出如图所示“浓差电池”(其电动势取决于物质的浓度差,是由一种物质从高浓度向低浓度转移而产生的)。其中,甲池为3mol·L-1的AgNO3溶液,乙池为1mol·L-1的AgNO3溶液A、B均为Ag电极。实验开始先断开K1,闭合K2,发现电流计指针发生偏转。下列说法不正确的是

A. 当电流计指针归零后,断开K2,闭合K1,一段时间后B电极的质量增加
B. 断开K1,闭合K2,一段时间后电流计指针归零,此时两池银离子浓度相等
C. 实验开始先断开K1,闭合K2,此时NO3-向B电极移动
D. 当电流计指针归零后,断开K2闭合K1,乙池溶液浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com