
| A. | c=$\frac{3b}{0.0224V}$ | B. | e=a+$\frac{8cV}{1000}$ | C. | d=a+$\frac{17cV}{1000}$ | D. | $\frac{82a}{65}$<e<$\frac{5a}{4}$ |
分析 根据题意利用反应过程中的变化进行分析计算,a g锌和铜的混合物中加入适量的稀硝酸全部反应生成标况下NO bL和硝酸锌、硝酸铜;向反应后的溶液中加入c mol/L氢氧化钠溶液V mL使金属离子刚好沉淀完全,得到的沉淀为氢氧化锌和氢氧化铜,质量为dg,固体灼烧得到氧化锌和氧化铜质量为eg,结合各步反应进行计算判断.
解答 解:反应化学方程式为:3Zn+8H++2NO3-(稀)═3Zn2++2NO↑+4H2O、3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O、Cu2++2OH-=Cu(OH)2↓、Zn2++2OH-=Zn(OH)2↓;Zn(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ZnO+H2O;Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
A.标况下bL一氧化氮的物质的量为:$\frac{bL}{22.4L/mol}$=$\frac{b}{22.4}$mol,金属离子恰好沉淀时消耗的氢氧根离子与金属与稀硝酸反应转移的电子的物质的量相等,则消耗氢氧化钠的物质的量为:$\frac{b}{22.4}$mol×3=$\frac{3b}{22.4}$mol,则氢氧化钠溶液的浓度为:$\frac{\frac{3b}{22.4}mol}{V×1{0}^{-3}L}$=$\frac{3b}{0.0224V}$mol/L,故A正确;
B.e为氧化锌、氧化铜的质量,则e为金属的质量+氧元素的质量,氧元素的物质的量是金属元素所带电荷物质的量的0.5倍,金属所带电荷与氢氧根离子的物质的量相等,则氧元素的物质的量为:cmol/L×0.001VL×$\frac{1}{2}$=$\frac{cV}{500}$mol,故氧化物的质量为:e=a+$\frac{cV}{500}$×16=a+$\frac{8cV}{1000}$,故B正确;
C.得到的氢氧化锌和氢氧化铜的质量等于混合金属的质量和与氢氧根离子的质量之和,即d=a+$\frac{17cV}{1000}$,故C正确;
D.氧化锌和氧化铜的质量可以按照极值方法计算,若mg全是锌,得到的氧化物为氧化锌,根据元素守恒,则质量为e=$\frac{a}{65}$×81=$\frac{81a}{65}$;若mg全是铜,得到的氧化物为氧化铜,根据元素守恒,则质量为e=$\frac{a}{64}$×80=$\frac{5}{4}$a;氧化锌和氧化铜的质量介于二者之间,即:$\frac{81a}{65}$<e<$\frac{5}{4}$a,故D错误;
故选D.
点评 本题考查混合物的计算,题目难度中等,侧重于物质的量应用于化学方程式的计算的考查,题目信息量较大,易错点为D,注意利用极值方法计算.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=13的溶液:K+、Na+、Cl-、SiO32- | |
| B. | c(H+)/c(OH-)=1×10-14的溶液:Na+、NH4+、Cl-、SO42- | |
| C. | 0.1mol•L-1的Na2CO3溶液:Na+、Ca2+、I-、SO42- | |
| D. | 加入石蕊呈蓝色的溶液:Na+、Al3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a g | B. | 0.5a g | C. | 4.4a g | D. | 1.8a g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
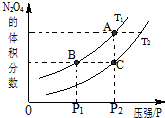 试运用所学知识,研究CO等气体的性质,请回答:
试运用所学知识,研究CO等气体的性质,请回答:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++H2O | |
| B. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某学生用pH试纸测新制氯水的pH值,先变红后褪色,是因为Cl2有强氧化性 | |
| B. | 容量瓶、分液漏斗、滴定管在使用前要检查是否漏水 | |
| C. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| D. | 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质的量浓度相等的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2三种溶液,c(NH4+)的大小顺序为:①>②>③ | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 0.2mol•L-1HCl与0.1mol•L-1NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com