
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$值增大 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 再加入10 mL pH=11的NaOH溶液,酸与碱恰好完全反应 |
分析 根据醋酸是弱电解质,则室温下向10mLpH=3的醋酸溶液中加水稀释将促进电离,离子的数目增多,但溶液的体积增大,则电离产生的离子的浓度减小,并利用温度与电离常数的关系、酸碱混合时pH的计算来解答.
解答 解:A.醋酸是弱酸,存在电离平衡.在醋酸溶液中加水稀释,促进电离,则液中导电粒子的数目增多,故A错误;
B.加水稀释时,c(H+)减小,因醋酸的电离平衡常数K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$不变,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$值增大,故B正确;
C.加水稀释时,电离程度增大,但溶液的体积增大的倍数大于n(H+)增加的倍数,则c(H+)减小,故C错误;
D.等体积10mLpH=3的醋酸与pH=11的NaOH溶液混合时,醋酸的浓度大于0.001mol/L,醋酸过量,故D错误.
故选B.
点评 本题考查弱电解质电离平衡的有关判断,是高考中的常见题型,属于中等难度的试题.主要是考查学生对弱电解质电离平衡特点以及外界条件对电离平衡影响的熟悉了解程度.答题明确温度与电离平衡常数的关系、溶液的pH与物质的量浓度的关系、稀释中溶液体积的变化与离子的物质的量的变化程度是解答本题的关键.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 制备Fe(OH)3胶体:向0.1mol•L-1FeCl3溶液中加入等体积0.3mol•L-1NaOH溶液 | |
| B. | 除去FeCl3溶液中少量Cu2+:向含有少量Cu2+的FeCl3溶液中加入适量铁粉,充分反应后过滤 | |
| C. | 比较Fe(OH)3和Al(OH)3的溶度积:向0.1mol•L-1FeCl3溶液中滴加0.1 mol•L-1氨水至不再产生沉淀,然后再滴入0.1mol•L-1AlCl3溶液,观察现象 | |
| D. | 验证氧化性Fe3+<Br2<Cl2:向试管中依次加入1mL 0.1mol•L-1FeBr2溶液、几滴KSCN溶液和1mL苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机相和水相中的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 由图甲知,A点SO2的平衡浓度为0.4 mol/L | |
| B. | 由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2 | |
| C. | 压强为0.50 MPa时不同温度下SO2转化率与温度关系如图乙,则T2>T1 | |
| D. | 达平衡后,缩小容器容积,则反应速率变化图象可以用图丙表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
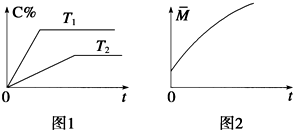 在密闭容器中投入一定量的A和B发生反应:
在密闭容器中投入一定量的A和B发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02mol/L醋酸溶液与等体积的水混合 | |
| B. | 0.02mol/L醋酸与0.02mol/LNaOH溶液等体积混合液 | |
| C. | 0.03mol/L醋酸与0.01mol/LNaOH溶液等体积混合液 | |
| D. | pH=2的盐酸与pH=12的NaOH溶液等体积混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一分子O4由两分子O2构成 | |
| B. | O4是一种单质 | |
| C. | 等质量的O4和O2含有相同数目的分子 | |
| D. | O4是一种化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com