


科目:高中化学 来源:四川省绵阳中学2011届高三化学考前热点训练:11 电解质溶液 题型:013
|
下列溶液中各微粒的浓度关系一定正确的是 | |
| [ ] | |
A. |
物质的量浓度相同的4种溶液①CH3COONa;②NaNO3;③Na2CO3;④NaOH,pH的大小顺序是:④>③>①>② |
B. |
在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO |
C. |
25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1∶1 |
D. |
某酸性溶液中只含NH c(Cl-)>c(NH |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省衡水市第十四中学高二下学期期末考试化学试卷(带解析) 题型:单选题
下列溶液中各微粒的浓度关系一定正确的是( )
A.某酸性溶液中只含NH 、Cl-、H+、OH-四种离子,溶液中一定存在: 、Cl-、H+、OH-四种离子,溶液中一定存在:c(Cl-)>c(NH  )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| B.物质的量浓度相同的4种溶液:①CH3COONa;②NaNO3;③Na2CO3;④NaOH, pH的大小顺序是:④>③>①>② |
C.在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO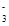 )+c(OH-)+c(CO )+c(OH-)+c(CO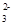 ) ) |
| D.25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1∶1 |
查看答案和解析>>
科目:高中化学 来源:2014届河北省衡水市高二下学期期末考试化学试卷(解析版) 题型:选择题
下列溶液中各微粒的浓度关系一定正确的是( )
A.某酸性溶液中只含NH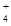 、Cl-、H+、OH-四种离子,溶液中一定存在:
、Cl-、H+、OH-四种离子,溶液中一定存在:
c(Cl-)>c(NH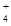 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.物质的量浓度相同的4种溶液:①CH3COONa;②NaNO3;③Na2CO3;④NaOH,
pH的大小顺序是:④>③>①>②
C.在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO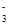 )+c(OH-)+c(CO
)+c(OH-)+c(CO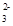 )
)
D.25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1∶1
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| H | +4 |
A.溶液中离子浓度可能满足:c(Cl-)>c(H+)>c(N
| ||
| B.该溶液不能由等物质的量浓度、等体积的盐酸和氨水混合而成 | ||
| C.可由pH=3的盐酸与pH=11的氨水等体积混合而成 | ||
D.再通入适量氨气,溶液中离子浓度可能为:c(N
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com