
【题目】I.一定量的CO(g)和H2O(g)分别通入容积为1L的恒容密闭容器中,发生反应CO(g)+H2OCO2(g)+H2(g)得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衝所需时间/min | |
CO | H2O | CO2 | |||
1 | 500 | 8 | 4 | 3.2 | 4 |
2 | 700 | 4 | 2 | 0.8 | 3 |
3 | 700 | 4 | 2 | 0.8 | 1 |
(1)①下列情况表明反应达到平衡状态的是 (填序号)
A.CO2和H2生成速率相等
B.温度不变时,压强不变
C.生成CO2的速率和生成CO的速率相等
②实验2中,反应达到平衡状态时,CO的转化率为 .
③实验3和实验2相比,改变的条件是 .
(2)①硫化钠溶液具有较强碱性,其原因是(用离子方程式表示).
②欲使0.1mol的Na2S溶液中, ![]() 的值增大,可采取的措施是(填序号)
的值增大,可采取的措施是(填序号)
A.加适量等浓度的NaOH溶液
B.加适量的水
C.通入适量的H2S气体.
【答案】
(1)C;20%;加催化剂
(2)S2﹣+H2O?HS﹣+OH﹣ , HS﹣+H2O?H2S+OH﹣;BC
【解析】解:I.(1)A.CO2和H2都作为生成物,根据反应可知,自始至终v正(CO2)=v正(H2),CO2和H2生成速率相等,不能说明反应到达平衡,故A错误;
B.反应前后气体的物质的量不发生变化,容器中始终压强不变,温度不变时,压强不变,不能说明反应到达平衡,故B错误;
C.根据反应可知,自始至终v正(CO)=v正(CO2),若v正(CO2)=v逆(CO),则v正(CO)=v逆(CO),即生成CO2的速率和生成CO的速率相等,说明反应到达平衡,故C正确;
所以答案是:C;(2)实验2中,反应达到平衡状态时,反应
CO(g)+ | H2O | CO2(g)+ | H2(g) | |
起始(mol) | 4 | 2 | 0 | 0 |
转化(mol) | 0.8 | 0.8 | 0.8 | 0.8 |
平衡(mol) | 3.2 | 1.2 | 0.8 | 0.8 |
CO的转化率= ![]() ×100%=
×100%= ![]() ×100%=20%,
×100%=20%,
所以答案是:20%; (3)催化剂能改变反应速率,但不能改变平衡,实验3和实验2相比,起始量、平衡量相同,达到平衝所需时间实验3所需的时间少,所以实验3改变的条件为加催化剂,
所以答案是:加催化剂;
II、(1)硫化钠是强碱弱酸盐,硫离子水解导致溶液呈碱性,氢硫酸为二元弱酸,其盐分步水解,水解方程式为:S2﹣+H2OHS﹣+OH﹣ , HS﹣+H2OH2S+OH﹣ ,
所以答案是:S2﹣+H2OHS﹣+OH﹣ , HS﹣+H2OH2S+OH﹣;(2)A.加入氢氧化钠溶液后,氢氧根离子浓度增大,抑制了硫离子的水解,则硫离子浓度增大、HS﹣的浓度减小,则该比值减小,故A错误;
B.加入适量水,导致S2﹣的水解程度增大,则S2﹣的物质的量减小,HS﹣的物质的量增大,由于在同一溶液中,则 ![]() 的值会增大,故B正确;
的值会增大,故B正确;
C.向溶液中适量H2S气体后,导致溶液中HS﹣的浓度增大,S2﹣的浓度减小,则 ![]() 的值会增大,故C正确;
的值会增大,故C正确;
所以答案是:BC.
【考点精析】本题主要考查了化学平衡状态本质及特征和化学平衡状态的判断的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法不正确的是( )
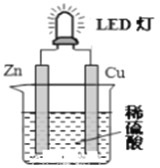
A. 铜片表面有气泡生成,且溶液中SO42-向该电极移动
B. 装置中存在“化学能→ 电能→ 光能”的转换
C. 如果将硫酸换成柠檬汁,导线中仍有电子流动
D. 如果将锌片换成铁片,电路中的电流方向不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于化合物的叙述中,正确的是
A. 活细胞中含量最多的化合物一般是蛋白质
B. 无机盐主要以化合物质形式存在
C. 脂质中具有良好储能作用的是胆固醇
D. 玉米叶肉细胞中有两种核酸,各含有4种核苷酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.离原子核越近的电子所具有的能量越低
B.一切原子都有质子和中子
C.稀有气体元素的原子最外层电子数都是 8 个
D.原子核外第n层上所排的电子数必定为2n2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,工业上合成尿素(H2NCONH2)的反应如下:2NH3(I)+CO2(g)H2O(I)+H2NCONH2(I)△H=﹣103.7kJmol﹣1试回答下列问题:
(1)写出一种有利于提高尿素的产率的措施是 .
(2)合成尿素的反应在进行时分为如下两步: 第一步:2NH3(I)+CO2(g)H2NCOONH4(I)(氨基甲酸铵)△H1
第二步:H2NCOONH4(I)H2O(I)+H2NCONH2(I)△H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.2L的密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图甲所示:
①●●代表的物质为(填化学式)
②已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第步反应决定,反应进行到10min时到达平衡.反应进行到10min时测得●●所代表的物质的量如图所示,则该物质表示的表示化学反应的速率为molL﹣1min.L﹣1
③第二步反应的平衡常数K2随温度的变化如乙图所示,则△H1 0 (填“>”“<”或“=”).
④第一步反应在(填“较高”或“较低”)温度下有利该反应自发进行.
(3)已知: N2(g)+O2(g)=2NO(g)△H=+180.6kJmol﹣1
N2(g)+3H2(g)=2NH3(g)△H=﹣92.4kJmol﹣1
2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJmol﹣1
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的工作原理如图所示。下列说法正确的是( )
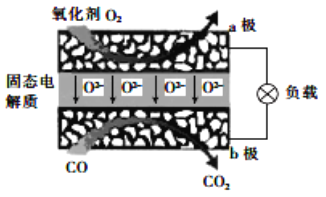
A. 正极的电极反应式为 O2+4e-+2H2O===4OH-
B. 还可以选用 NaOH 固体作固态电解质
C. 若反应中转移 1 mol 电子,则生成 22.4LCO2
D. 电子从 b 极经导线流向 a 极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是( )
A.酒精、冰醋酸、纯碱均为电解质B.硅酸、稀豆浆、氯化铁溶液均为胶体
C.碘酒、食盐水、氨水均为混合物D.SO2、SiO2、CO均为酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有碳等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )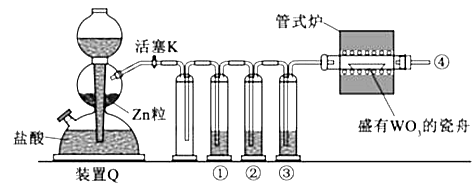
A.①、②、③中依次盛装KMNO4溶液、浓H2SO4、焦性没食子酸溶液
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com