
分析 原子序数依次增大的 A、B、C、D、E五种短周期主族元素,A、B、C分布于三个不同的周期中,则A为H,B为第二周期元素,C为第三周期元素;D的原子序数是B的两倍,元素D的单质在反应中能置换出元素B的单质,则D为Mg,B为C,结合原子序数可知C为Na,E是同周期元素原子半径最小的元素,则E为Cl,然后结合元素周期律及元素化合物知识来解答.
解答 解:原子序数依次增大的 A、B、C、D、E五种短周期主族元素,A、B、C分布于三个不同的周期中,则A为H,B为第二周期元素,C为第三周期元素;D的原子序数是B的两倍,元素D的单质在反应中能置换出元素B的单质,则D为Mg,B为C,结合原子序数可知C为Na,E是同周期元素原子半径最小的元素,则E为Cl,
(1)B在元素周期表的位置为第二周期、第VIA族,故答案为:第二周期、第VIA族;
(2)A与C形成化合物的电子式为Na+[:H]-;该化合物与水反应的化学方程式是 NaH+H2O=NaOH+H2↑,故答案为:Na+[:H]-;NaH+H2O=NaOH+H2↑;
(3)D的单质置换出B的单质的方程式为2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(4)H有+1价,可在IA族,H有-1价,可在VⅡA族,且最高正价与最低负价倒数和为0,可在ⅣA族,故答案为:IA;VⅡA;ⅣA.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的位置推断元素为解答的关键,侧重分析与推断能力的考查,注意周期律及元素化合物知识的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
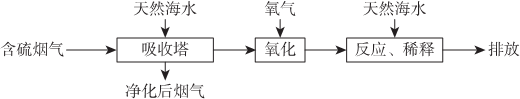
| A. | 天然海水pH≈8的原因是由于海水中的CO32-、HCO3-水解 | |
| B. | “氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42- | |
| C. | “反应、稀释”时加天然海水的目的是防止净化海水时生成沉淀 | |
| D. | “排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |||
| Z | W | Q |
| A. | Z位于第3周期 IIIA族 | |
| B. | X、Z、W、Q等元素的最高正价等于其所在族的族序数 | |
| C. | Y元素气态氢化物比W元素的气态氢化物更稳定,是因为前者分子间形成了氢键 | |
| D. | X的最高价氧化物对应的水化物和X的氢化物形成的化合物含有离子键、共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
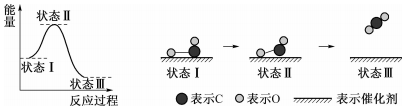
| A. | 状态Ⅰ→状态Ⅲ是放热过程 | |
| B. | 该过程中,CO没有断键形成C和O | |
| C. | 状态Ⅰ→状态Ⅲ表示CO和O生成了CO2 | |
| D. | 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 沸点/℃ | 物质 | 沸点/℃ |
| 溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
| 苯甲醛 | 179 | 间溴苯甲醛 | 229 |
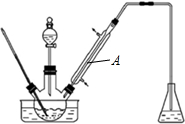
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F、Cl、Br、I最高正化合价都为+7 | |
| B. | 卤族元素的单质只有氧化性 | |
| C. | 从F到I,原子的得电子能力依次减弱 | |
| D. | 卤素单质与H2化合的难易程度按F2、Cl2、Br2、I2的顺序由难变易 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 | |
| 实验1 | 3.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 实验2 | 1.5mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
| 实验3 | 3.0mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com