
| AӢH+ӢI-ӢNO3-ӢSiO32- |
| BӢK+ӢSO42-ӢCu2+ӢNO3- |
| CӢAg+ӢFe3+ӢCl-ӢSO42- |
| DӢNH4+ӢOH-ӢCl-ӢHCO3- |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŹµŃé | ¼× | ŅŅ | ±ū |
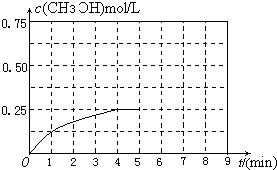
| ³õŹ¼Ķ¶ĮĻ | 2molH2”¢1molCO | 1mol CH3OH | 4molH2”¢2molCO |
| Ę½ŗāŹ±n£ØCH3OH £© | 0.5mol | n2 | n3 |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | ·Å³öQ1kJ | ĪüŹÕQ2kJ | ·Å³öQ3kJ |
| ĢåĻµµÄŃ¹Ēæ | P1 | P2 | P3 |
| ·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ | ¦Į1 | ¦Į2 | ¦Į3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
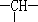 ŗĶŅ»øö-Cl£¬ĖüµÄæÉÄܵĽį¹¹ÓŠ¼øÖ֣ؔ”””£©
ŗĶŅ»øö-Cl£¬ĖüµÄæÉÄܵĽį¹¹ÓŠ¼øÖ֣ؔ”””£©| A”¢2 | B”¢3 | C”¢4 | D”¢5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
AӢ
| ||
BӢ
| ||
CӢ
| ||
DӢ
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| Ń”Ļī | »·¾³ŅŖĒó | Ąė×Ó |
| A | ČÜŅŗÖŠc£ØK+£©£¼c£ØCl-£© | K+”¢AlO2-”¢Cl-”¢NO3- |
| B | ČÜŅŗpH£¾7 | Na+”¢S2-”¢K+”¢ClO- |
| C | Ė®µēĄė²śÉśµÄc£ØH+£©=10-12 mol/LµÄČÜŅŗ | ClO-”¢CO32-”¢NH4+”¢NO3-”¢SO32- |
| D | ĻņČÜŅŗÖŠÖšµĪµĪ¼ÓÉÕ¼īČÜŅŗĻČÓŠ³Įµķ²śÉś£¬ŗó³ĮµķĻūŹ§ | Na+”¢Al3+”¢Cl-”¢SO42- |
| AӢA | BӢB | CӢC | DӢD |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢MgCl2¾§Ģå |
| B”¢NaClČÜŅŗ |
| C”¢ŅŗĢ¬¾Ę¾« |
| D”¢ČŪČŚµÄKOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ĪĀ¶Č”¢ČŻ»ż²»±äŹ±£¬ĶØČėSO2ĘųĢå |
| B”¢ŅĘ×ßŅ»²æ·ÖNH4HS¹ĢĢå |
| C”¢ČŻ»ż²»±ä£¬³äČė°±Ęų |
| D”¢±£³ÖŃ¹Ēæ²»±ä£¬³äČėµŖĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ŅŅĻ©µÄ½į¹¹¼ņŹ½ĪŖCH2CH2 |
B”¢ōĒ»łµÄµē×ÓŹ½£ŗ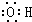 |
C”¢±ūĻ©µÄ¼üĻߏ½£ŗ |
| D”¢ŅŅ“¼µÄ·Ö×ÓŹ½£ŗCH3CH2OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com