
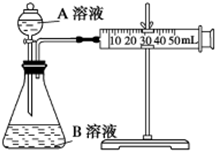
 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ② | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液和少量MnSO4 |
分析 (1)高锰酸根离子在酸性条件下氧化草酸生成锰离子、二氧化碳气体和水,据此写出反应的离子方程式;
(2)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大;对比②③实验可探究催化剂对化学反应速率的影响,③中使用了催化剂;
(3)草酸和高锰酸钾反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,分析可知没有加入稀硫酸酸化或高锰酸钾过量导致.
解答 解:(1)KMnO4酸性溶液与H2C2O4溶液反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,
对比②③实验可探究催化剂对化学反应速率的影响,③中使用了催化剂,故相同时间内③的反应速率最快,实验中所得二氧化碳最多,
所以该实验目的为探究浓度和催化剂对反应速率的影响;在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序为:③>②>①,
故答案为:浓度和催化剂; ③>②>①;
(3)草酸和高锰酸钾反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
草酸的物质的量为:0.002L×0.1mol•L-1=2×10-4mol,
高锰酸钾的物质的量为:0.004L×0.1mol•L-1=4×10-4mol,
由方程式可知,没有加入稀硫酸酸化或高锰酸钾过量,故没看到溶液完全褪色,
故答案为:温度;没有加入稀硫酸酸化或高锰酸钾过量导致.
点评 本题考查了探究影响化学反应速率的因素方法,题目难度中等,注意掌握浓度、温度、催化剂对化学反应速率的影响,试题侧重考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.77×10-4 | 4.9×10-16 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | HCOOH+CN-═HCOO-+HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入氢气的电极为原电池的正极 | |
| B. | 两极材料都用石墨,用稀盐酸做电解质溶液 | |
| C. | 电解质溶液中的阳离子向通氯气的电极移动 | |
| D. | 通氯气的电极反应式为Cl2+2e-═2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2、NaHCO3均可能与强酸、强碱反应,都为两性物质 | |
| B. | Na2CO3、CH3COOH、Cu2(OH)2CO3均含有碳元素,都是有机化合物 | |
| C. | BaCO3、BaSO3、BaSO4均难溶于水,均属于难溶电解质 | |
| D. | HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,4.48LCHCl3的分子数为0.2 NA | |
| B. | 常温常压下,8gCH4含有5NA个电子 | |
| C. | 6.0g冰醋酸与4.6g乙醇反应生成乙酸乙酯的分子数为0.1 NA | |
| D. | 28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -OH与OH-具有相同的质子数 | |
| B. | 在葡萄糖溶液中加入银氨溶液,一会儿就会看到光亮的银析出 | |
| C. | 检验乙醇中是否含有水可用无水硫酸铜 | |
| D. | 某有机物在氧气中燃烧生成CO2和H2O,则该有机物可能是烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 德国的维勒 | B. | 瑞典的贝采里乌斯 | ||
| C. | 德国的李比希 | D. | 匈牙利的海维西 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com