
计算题(本题包括1小题,共10分)
22.取100mL的Na2CO3和Na2SO4混合溶液,加入Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算:[第(3)问请写出计算过程]
(1)原混合液中Na2SO4的物质的量浓度为 mol ·L-1;
(2)产生的气体在标准状况下的体积为 L;
(3)过滤出沉淀后,计算所得滤液的物质的量浓度?
(设反应前后溶液的密度均为1g·cm-3,反应前后溶液体积变化忽略不计)。
(1)0.2 (2)1.12
(3)所得滤液溶质为NaOH。根据Na元素守恒得
n(NaOH)=2×[n(Na2SO4)+n(Na2CO3)]=2×[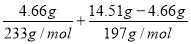 ]=0.14mol
]=0.14mol
故 c(NaOH)=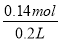 =0.7mol/L
=0.7mol/L
【解析】
试题分析:由题意可知,100mL的Na2CO3和Na2SO4混合溶液,加入Ba(OH)2溶液100 mL后,恰好完全反应,产生沉淀为BaSO4与BaCO3的混合物14.51g,再用过量稀硝酸处理沉淀,BaCO3溶于HNO3,而BaSO4不溶,则剩余4.66g沉淀为BaSO4,故可得n(SO42—)=4.66g/233g/mol=0.02mol,则原混合液中Na2SO4的物质的量浓度为=0.02mol/0.1L=0.2mol/L,则m(BaCO3)=14.51g-4.66g=9.85g,n(CO32-)=9.85g/197g/mol=0.05mol,n(CO2)=0.05mol,V(CO2)=0.05mol×22.4L/mol=1.12L;由质量守恒定律钠元素守恒可知溶液中有n(Na+)=(0.02+0.05)×2=0.14mol,恰好完全反应后的溶液溶质为NaOH溶液,故c(NaOH)=0.14mol/0.2L=0.7mol/L。
考点:元素及其化合物计算。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高一上第一次考试化学(A)试卷(解析版) 题型:选择题
下列溶液中的氯离子数目与50 mL 1 mol/L的AlCl3溶液中氯离子数目相等的是( )
A.150 mL 2 mol/L的NaCl溶液 B.75 mL 2 mol/L的NH4Cl溶液
C.150 mL 3 mol/L的KCl溶液 D.75 mL 2 mol/L的CaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上第二次考试化学试卷(解析版) 题型:选择题
在物质分类中,前者包括后者的是( )。
A.氯化物、化合物 B.化合物、电解质
C.溶液、胶体 D.溶液、 分散系
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高二上学期期中化学试卷(解析版) 题型:选择题
食品包装袋中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反映,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池负极,电极反应为:Fe-3e-==Fe3+
C.脱氧过程中碳做原电池正极,电极反应为: O2+4 e-+4H+== 2H2O
D.含有2.24g铁粉的脱氧剂,理论上最多能吸收氧气672 mL(标准状况)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高二上学期期中化学试卷(解析版) 题型:选择题
下表中与化学反应相对应的方程式中,正确的是
选项 | 化学反应 | 离子方程式 |
A | 以石墨作电极电解氯化钠溶液 | 2Cl- + 2H2O |
B | 以银作电极电解硝酸银溶液 | 4Ag++2H2O = 4Ag+O2↑ +4H+ |
C | 铅蓄电池正极反应 | PbO2+4H++2e- === Pb2++2H2O |
D | 氢氧燃料电池(KOH做电解液)负极反应 | O2 + 4e-+ 2H2O = 4OH- |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上学期期中化学试卷(解析版) 题型:选择题
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5 mol/L,Mg2+为0.5 mol/L,则SO42-的物质的量浓度为
A.0.1 mol/L B.0.5 mol/L
C.0.15 mol/L D.0.25 mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上学期期中化学试卷(解析版) 题型:选择题
下列有关胶体叙述不正确的是
A.实验室用于鉴别胶体与溶液的方法是丁达尔现象
B.豆浆制豆腐是利用了胶体聚沉的原理
C.氢氧化铁胶体微粒带正电,通电时胶体微粒向直流电源正极移动
D.分散质微粒介于1~100nm之间的分散系称为胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高二10月月考化学试卷(解析版) 题型:选择题
在密闭容器中发生如下反应: aX(g) + bY(g) 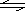 cZ(g) +d W(g)。反应达平衡后保持温度不变,将气体体积压缩到原来的1/2,当再次达平衡时,W的浓度为原平衡时的1.8倍。下列叙述中不正确的是 ( )
cZ(g) +d W(g)。反应达平衡后保持温度不变,将气体体积压缩到原来的1/2,当再次达平衡时,W的浓度为原平衡时的1.8倍。下列叙述中不正确的是 ( )
A.平衡向逆反应方向移动 B.a + b < c + d
C.Z的体积分数增加 D.X的转化率下降
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省汝州市高二上学期第一次月考化学试卷(解析版) 题型:填空题
已知下列热化学方程式:①H2(g) + O2 (g) =H2O(l);ΔH=-285 kJ·mol-1
O2 (g) =H2O(l);ΔH=-285 kJ·mol-1
②H2(g) + O2 (g) =H2O(g);ΔH=-241.8 kJ·mol-1
O2 (g) =H2O(g);ΔH=-241.8 kJ·mol-1
③C(s) + O2 (g) =CO(g);ΔH=-110.5 kJ·mol-1
O2 (g) =CO(g);ΔH=-110.5 kJ·mol-1
④ C(s) +O2 (g) =CO2(g);ΔH=-393.5 kJ·mol-1
回答下列问题:
(1)H2的燃烧热为 C的燃烧热为 。
(2)燃烧10gH2生成液态水,放出的热量为 。
(3)写出CO燃烧的热化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com