
分析 (1)氯气与消石灰发生反应生成CaCl2和Ca(ClO)2的混合物,有效成分是Ca(ClO)2,它之所以能消毒杀菌是因有强的氧化性;
(2)KAl(SO4)2•12H2O的俗名为明矾,该盐是强酸弱碱盐,电离产生的Al3+与水电离产生的OH-结合形成表面积比较大的Al(OH)3胶体而有吸附作用,使水中悬浮的固体被吸附;
(3)CO2溶于水形成碳酸,饱和碳酸溶液的pH=5.6,当水中溶解SO2、NO2等气体时,使溶液的酸性增强,pH减小,因此就把pH<5.6的酸性降水称为酸雨.含亚硫酸的酸雨久置后,会和空气中的氧气发生反应:2H2SO3+O2=2H2SO4;
(4)NaHCO3与胃酸即盐酸发生复分解反应,产生CO2和水;
(5)溴单质为红棕色液体.
解答 解:(1)氯气与消石灰发生反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,产生漂白粉,漂白粉的成分是CaCl2和Ca(ClO)2的混合物,有效成分是Ca(ClO)2,它之所以能消毒杀菌是因有强的氧化性,
故答案为:Ca(ClO)2;氧化性;
(2)KAl(SO4)2•12H2O的俗名为明矾,该盐是强酸弱碱盐,电离产生的Al3+与水电离产生的OH-结合形成表面积比较大的Al(OH)3胶体而有吸附作用,使水中悬浮的固体被吸附,当重力大于浮力时,就形成沉淀,从而使水变得澄清,因此有净水作用,
故答案为:明矾;Al(OH)3;
(3)CO2溶于水形成碳酸,饱和碳酸溶液的pH=5.6,当水中溶解SO2、NO2等气体时,使溶液的酸性增强,pH减小,因此就把pH<5.6的酸性降水称为酸雨.含亚硫酸的酸雨久置后,会和空气中的氧气发生反应:2H2SO3+O2=2H2SO4,H2SO3是弱酸,而H2SO4是强酸,因此酸雨久置,溶液中c(H+)增大,pH减小,
故答案为:5.6;减小;
(4)NaHCO3与胃酸即盐酸发生复分解反应,产生CO2和水,反应的离子方程式是:HCO3-+H+=CO2↑+H2O,故答案为:HCO3-+H+=CO2↑+H2O;
(5)溴单质的颜色为红棕色液体,故答案为:红棕色.
点评 本题考查物质的成分、作用、俗称、化学式和离子方程式的书写的知识,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | ①>②>③ | B. | ②>①>③ | C. | ③>①>② | D. | ②>③>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 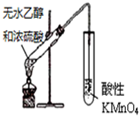 A装置用于检验乙醇发生消去反应的产物 | |
| B. | 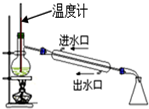 B装置可用于分离乙醇和丙三醇形成的混合物 | |
| C. | 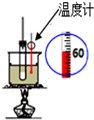 C装置用于实验室制硝基苯 | |
| D. | 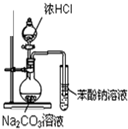 D装置可证明酸性:盐酸>碳酸>苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制Fe(OH)3胶体 | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用蒸发皿进行加热蒸发实验时,不需要垫石棉网 | |
| B. | 蒸馏时,应将温度计水银球插入液面以下 | |
| C. | 闻气味时,应用手在容器口轻轻扇动,使少量气体飘入鼻孔中 | |
| D. | 使用分液漏斗和容量瓶时,都要首先检查是否漏水 | |
| E. | 分液时,先把分液漏斗中上层液体从上口倒出,再把下层液体从下口放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中溶剂与溶质的质量比为m(水):m(溶质)=( $\frac{18na}{M}$+b):(a-$\frac{18na}{M}$) | |
| B. | 该溶液的物质的量浓度为c=$\frac{1000a}{MV}$mol•L-1 | |
| C. | 该溶液中溶质的质量分数为ω=$\frac{100a(M-18n)}{a+b}$% | |
| D. | 该溶液的密度为ρ=$\frac{1000(a+b)}{V}$g•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2NaBr+Cl2═2NaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2═2H2O+3S↓ | |
| D. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com