
亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀菌。以下是用过氧化氢法生产亚氯酸钠的工艺流程图:

已知:NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
(1)吸收塔内发生反应的化学方程式为_____________________(配平化学方程式)。该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2。若用二氧化氯和浓盐酸制取Cl2,当生成5 mol Cl2时,通过还原反应制得氯气的质量为________克。
(2)从滤液中得到的NaClO2·3H2O晶体的操作依次是__________(填写序号)。
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时HClO2 及几种常见弱酸的电离平衡常数:

①常温下,物质的量浓度相等的NaClO2 、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为____________;体积相等,物质的量浓度相同的NaF、NaCN两溶液中所含阴阳离子总数的大小关系为:______________(填“前者大”“相等”或“后者大”)。
②Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+ 离子,滴加Na2S溶液后首先析出的沉淀是_______;当最后一种离子沉淀完全时(该离子浓度为10-5mol·L-1)此时的S2-的浓度为____。
已知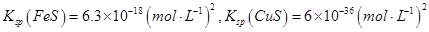

(14分)(1)2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2↑ 71(每空2分,共4分)(2)dc(2分)
(3)①Na2S>NaCN>NaF>NaClO2 前者大(每空2分,共4分)
②CuS 6.3×10-13mol/L(每空2分,共4分)
【解析】
试题分析:(1)根据流程信息可知,吸收塔内生成NaClO2,所以一定有ClO2→NaClO2,化合价降低,被还原;则H2O2必定被氧化,有氧气产生,因此反应的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2↑;二氧化氯和浓盐酸制取Cl2时,二氧化氯中氯元素的化合价从+4价降低到0价,得到4个电子。氯化氢中氯元素的化合价从-1价升高到0价,失去1个电子,则根据电子的得失守恒可知,氧化剂和还原剂大的物质的量之比是1:4,还原产物和氧化产物的物质的量之比也是1:4。因此当生成5 mol Cl2时,通过还原反应制得氯气的物质的量是1mol,质量为71g。
(2)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体,所以操作顺序为dc。
(3)①酸越弱,相应的钠盐越容易水解,溶液的碱性越强,pH越大。酸的电离平衡常数越小,酸越弱,所以根据电离平衡常数可知,酸性强弱顺序是HClO2>HF>H2S>HCN>HS-,则常温下,物质的量浓度相等的NaClO2 、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为Na2S>NaCN>NaF>NaClO2;根据电荷守恒可知在NaF、NaCN两溶液中存在c(Na+)+c(H+)=c(OH-)+c(F-)、c(Na+)+c(H+)=c(OH-)+c(CN-),因此两溶液中所含阴阳离子总数分别是n(Na+)+n(H+)+n(OH-)+n(F-)=2 n(Na+)+2n(H+)、n(Na+)+n(H+)+n(OH-)+n(CN-)=2 n(Na+)+2n(H+)。在物质的量浓度相等的条件下,NaF溶液的碱性弱于NaCN溶液的碱性,则NaF溶液中氢离子的浓度大于NaCN溶液中氢离子的浓度,因此积相等,物质的量浓度相同的NaF、NaCN两溶液中所含阴阳离子总数的大小关系为前者大。
②根据溶度积常数可知,CuS的溶度积常数最小,所以向含有等浓度的Cu2+、Fe2+、Pb2+
离子的溶液中,滴加Na2S溶液后首先析出的沉淀是CuS。最后析出的是FeS沉淀,当溶液中c(Fe2+)=10-5mol/L时,根据FeS的溶度积常数可知,溶液中c(S2-)= =6.3×10-13mol/L。
=6.3×10-13mol/L。
考点:考查氧化还原反应方程式的配平、计算;物质的分离与提纯;弱电解质的电离、盐类水解以及溶液中离子浓度大小比较;溶度积常数的应用和计算等


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 (2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、Cl
(2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、Cl| O | - 3 |
| O | - 3 |
| O | n- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 压强MPa 转化率% 温度℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
查看答案和解析>>
科目:高中化学 来源:2012届福建省三明市普通高中高三上学期联合命题考试化学试卷 题型:填空题
(10分)氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2 + H2O  HCl + HClO K=4.5×10-4
HCl + HClO K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为 。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为 。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧
化性强弱的微型装置(如图)。
①下列溶液能吸收Cl2的是 (填字母序号)。
| A.饱和食盐水 | B.饱和Na2SO3溶液 |
| C.饱和NaOH溶液 | D.浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年贵州省铜仁市高三第四次月考理综化学试卷(解析版) 题型:选择题
已知向氯酸钠的酸性水溶液中通入二氧化硫气体,反应中SO2氧化过程为:SO2+2H2O –2e- =SO42-+4H+;向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,反应中还原过程为:Cl2 + 2 e- =2Cl-。在上述两个反应中均会生成产物X,则X的化学式为( )
A.ClO2 B.NaClO4 C.HClO D. NaClO
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省三明市高三上学期联合命题考试化学试卷 题型:填空题
(10分)氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2 + H2O
 HCl
+ HClO K=4.5×10-4
HCl
+ HClO K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为 。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为 。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧
化性强弱的微型装置(如图)。

①下列溶液能吸收Cl2的是 (填字母序号)。
A. 饱和食盐水 B. 饱和Na2SO3溶液
C. 饱和NaOH溶液 D. 浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com