
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是__________,F元素的原子基态价层电子排布式为__________。
(2)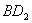 分子的电子式为__________,
分子的电子式为__________,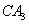 分子的空间立体构型为__________。
分子的空间立体构型为__________。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________、I:__________。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________。
(5)0.3g H在足量氧气中燃烧,生成气态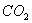 和液态
和液态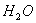 ,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。
,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。
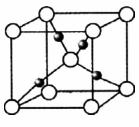
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________。
科目:高中化学 来源: 题型:
取pH值均等于2的盐酸和醋酸各120ml分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋分别与锌反应的速度一样大
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学课外小组用右图装置制取溴苯并探
某化学课外小组用右图装置制取溴苯并探
究该反应的类型。先向分液漏斗中加入苯和液溴,
再将混合液滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:_____________
_________________________________。
(2)实验结束时,打开A下端的活塞,让反应
液流入B中,充分振荡,目的是________
___________________________________。
(3)C中盛放CCl4的作用是_______________
__________________________________。
(4)若要证明苯和液溴发生的是取代反应,而不
是加成反应,通常有两种方法,请按要求填
写下表。
| 向试管D中加入的试剂 | 能证明苯与液溴发生取代反应的现象 | |
| 方法一 | ||
| 方法二 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A. 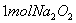 固体中含离子总数为
固体中含离子总数为
B. 常温下,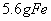 与足量稀
与足量稀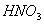 反应,转移
反应,转移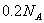 个电子
个电子
C. 常温常压下,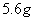 乙烯与丁烯的混合物中含有的氢原子的数目为
乙烯与丁烯的混合物中含有的氢原子的数目为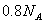
D. 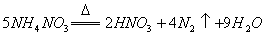 反应中,生成
反应中,生成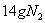 时,转移的电子数目为
时,转移的电子数目为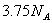
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应2AB(g) C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的正反应的ΔH、ΔS应为( )
C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的正反应的ΔH、ΔS应为( )
A. ΔH<0,ΔS>0 B. ΔH<0,ΔS<0 C. ΔH>0,ΔS>0 D. ΔH>0,ΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:
Ag2SO4(s) Ag2O(s)+SO3(g) 2SO3(g)
Ag2O(s)+SO3(g) 2SO3(g) 2SO2(g)+O2(g)
2SO2(g)+O2(g)
经10分钟反应达到平衡,此时c(SO3)=0.4 mol/L,c(O2)=0.05 mol/L,下列叙述不正确的是( )
A.SO3的分解率为20% B.10分钟内ν(SO2)=0.01mol/(L·min)
C.容器内气体的密度为40g/L D.加压,容器内固体的质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
从物质A的水溶液出发,有如图所示的一系列变化(参加反应或反应生成的H2O没有表示出来)。
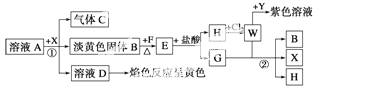
试完成下列问题:
(1)写出下列物质的化学式:
A________,E________,X________,Y________。
 (2)写出步骤①②发生反应的离子方程式:
(2)写出步骤①②发生反应的离子方程式:
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2 +12H2O====7Cu2S+5FeSO4 +12H2SO4。下列说法正确的是 ( )
A. Cu2S既是氧化产物又是还原产物
B. 5 mol FeS2发生反应,有12 mol电子转移
C. 产物中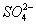 有一部分是氧化产物
有一部分是氧化产物
D. FeS2只作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com