
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展做出巨大贡献的科学家,锂离子电池广泛应用于手机、笔记本电脑等。
(1)锂元素在元素周期表中的位置:_________________。
(2)氧化锂(Li2O)是制备锂离子电池的重要原料,氧化锂的电子式为_____________。
(3)近日华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出了石墨烯电池,电池反应式为LIxC6+Li1-x![]() C6+LiCoO2,其工作原理如图。
C6+LiCoO2,其工作原理如图。
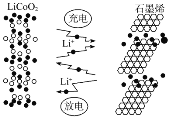
①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,层与层之间存在的作用力是_______。
②锂离子电池不能用水溶液做离子导体的原因是___________(用离子方程式表示)。
③锂离子电池放电时正极的电极反应式为________________。
④请指出使用锂离子电池的注意问题____________________。(回答一条即可)
【答案】第二周期第IA族 ![]() 范德华力(分子间作用力) 2Li+2H2O=2Li++2OH-+H2↑ Li1-xCoO2+xLi++xe-= LiCoO2 避免过充、过放、过电流、短路及热冲击或使用保护元件等
范德华力(分子间作用力) 2Li+2H2O=2Li++2OH-+H2↑ Li1-xCoO2+xLi++xe-= LiCoO2 避免过充、过放、过电流、短路及热冲击或使用保护元件等
【解析】
(1)根据锂元素的原子结构与元素位置的关系分析判断;
(2)氧化锂是离子化合物,Li+与O2-之间通过离子键结合;
(3)①石墨烯结构是平面结构,层内是共价键,层间以分子间作用力结合;
②根据Li是碱金属元素,利用碱金属单质的性质分析;
③锂离子电池放电时正极上Li+得电子变为LiCoO2;
④使用锂离子电池的注意问题是禁止过充、过房,配备相应的保护元件等。
(1)Li是3号元素,核外电子排布为2、1,所以Li在元素周期表的位置位于第二周期第IA族;
(2) Li2O是离子化合物,Li+与O2-之间通过离子键结合,其电子式为:![]() ;
;
(3)①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,在层内,C原子之间以共价键结合,在层与层之间存在的作用力是分子间作用力,也叫范德华力;
②Li是碱金属元素,单质比较活泼,容易和水反应产生氢气,反应方程式为:2Li+2H2O=2Li++2OH-+H2↑,所以锂离子电池不能用水溶液;
③根据锂电池总反应方程式可知:锂离子电池在放电时,正极上Li+得电子变为LiCoO2,电极反应式为:Li1-xCoO2+xLi++xe-= LiCoO2;
④锂电池在使用时应该注意的问题是避免过充、过放、过电流、短路及热冲击或使用保护元件等。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】(1)常温下,0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,则:
①混合溶液中由水电离出的c(H+)________(填“>”、“<”或“=”)HCl溶液中由水电离出的c(H+)。
②求出混合溶液中下列算式的精确计算结果(填具体数字)。c(Cl-)-c(M+)=________ mol·L-1;c(H+)-c(MOH)=________ mol·L-1。
(2)有A、B、C、D四种一元酸溶液,对它们进行的有关实验及其结果分别为:①在物质的量浓度相同的A、C两溶液中,都滴加几滴甲基橙时,A溶液呈黄色,C溶液呈橙色,②B的钠盐溶液的pH值小于C的钠盐溶液pH值,③A酸与D的盐反应生成A的盐和D酸。由此可以确定这四种酸的酸性由强到弱的正确排列顺序为 ________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 为阿伏加德罗常数的值,下列说法正确的是( )
A.1mol SiO2 所含Si-O键的数目为 2 NA
B.常温下,1 L pH=9的CH3COONa 溶液中由水电离的H+ 数目为 10-9 NA
C.40 mL 10 mol/L浓盐酸与足量MnO2充分反应,生成的氯气分子数为 0.1NA
D.标准状况下,11.2 L 甲烷和乙烯混合物中含氢原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.pH =1的H2SO4溶液中SO42-的数目为0.5NA
B.1 mol金刚石中C-C数目为4NA
C.12.0 g NaHSO4晶体中阴阳离子数目为0.3NA
D.2.3 g Na与过量O2反应转移电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应。下列分析正确的是
容器编号 | 实验条件 | 平衡时反应中的能量变化 |
I | 恒温恒容 | 放热Q1kJ |
II | 恒温恒压 | 放热Q2kJ |
Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Q1<Q2B.N2的转化率:I>Ⅲ
C.平衡常数:II>ID.平衡时氨气的体积分数:I>II
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表的另一种画法——塔式周期表,上面标有部分族及部分元素。请根据周期表中所列的元素回答问题:
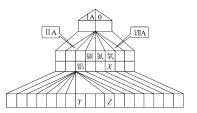
(1)碳、氮、氧三种元素的电负性由小到大的顺序为_____________________。
(2)Y3+的结构示意图为_____________,Z的价电子排布式为_______________。
(3)原子簇是由几个到几百个原子组成的相对独立的物质结构单元,如铝原子簇Al13、Al14。已知原子簇价电子总数为2,8,20,34,40,58……时,原子簇可稳定存在。
①Al13的化学性质与第__________族元素性质相似
②Al14达到稳定时,呈现的化合价为+2,其原因是___________________。

(4)某种化合物由X、Y、Z三种元素组成,其晶胞结构如图所示,则其化学式为____________,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:ρ=_______gcm-3(只要求列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml0.01mol/L CH3COOH溶液中逐滴加入0.01mol/LKOH溶液,其pH变化曲线如图所示(忽略温度和溶液体积的变化),下列说法正确的是( )
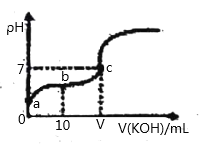
A.a点溶c(H+)为4.0×10-5mol/L
B.b点溶液中满足c(CH3COO-) +c(OH-)=c(CH3COOH)+c(H+)
C.V=20
D.滴定过程中,c(CH3COO-)+c(CH3COOH)+c(K+)=0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 稀硫酸溶液与氢氧化钡溶液恰好中和: Ba2++OH﹣+H++SO42﹣=BaSO4↓+H2O
B. 金属钠投入硫酸镁溶液中: 2Na+2H2O +Mg2+=2Na++H2↑+Mg(OH)2↓
C. 碳酸钠溶液中通入过量氯气: CO32﹣+Cl2=CO2↑+Cl-+ClO-
D. 实验室用 MnO2 和浓盐酸制取 Cl2: MnO2+4HCl(浓) ![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正x(CH3COOCH3)x(C6H13OH),v逆=k逆x(CH3COOC6H13)x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)反应开始时,已醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的ΔH____0(填>或<)。348K时,以物质的量分数表示的化学平衡常数Kx=____(保留2位有效数字)。在曲线①、②、③中,k正-k逆值最大的曲线是____;A、B、C、D四点中,v正最大的是___,v逆最大的是____。
(2)343K时,己醇和乙酸甲酯按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比____时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx___(填增大、减小或不变)。
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是____。
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com