
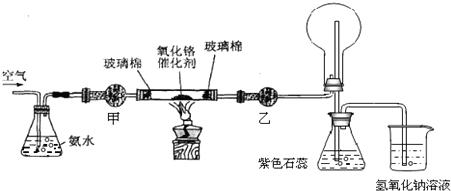
分析 (1)氨的催化氧化需要氧气,通入空气且利用氨气挥发;
(2)甲处是干燥氨气需要用碱石灰,乙处是干燥一氧化氮气体用氯化钙;氨气不能用氯化钙干燥;
(3)氨气的催化氧化生成一氧化氮和水,反应是放热反应;
(4)依据一氧化氮和二氧化氮被氢氧化钠溶液吸收生成的盐分析判断,NaNO2、NaNO3,可知钠元素和氮元素守恒,结合质量列式计算得到;
(5)缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生白烟.是因为氮氧化物和空气混合通入水中反应生成硝酸和过量氨气生成硝酸铵固体小颗粒.
解答 解:(1)氨气的催化氧化需要氧气作为氧化剂,且需要气体氨气,故需要氨气挥发,故答案为:提供氧气,且促进氨气的挥发;
(2)甲处是干燥氨气需要用碱石灰,防止水蒸气进入玻璃管炸裂玻璃管,乙处是干燥一氧化氮气体用氯化钙,不吸收后再后续装置会生成白烟;氨气不能用氯化钙干燥;甲处:碱石灰;乙处:无水氯化钙;故答案为:碱石灰;氯化钙;
(3)实验时,先将催化剂加热至红热,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,反应是放热反应,发生的是氨气的催化氧化反应生成一氧化氮和水,反应的化学方程式为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,故答案为:放热反应;4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;
(4)实验前,烧杯中盛有200mL 1.000mol/L的 NaOH溶液,实验后测得烧杯中溶液的pH=13,氢氧根离子浓度为0.1mol/L,且溶液质量比反应前增加了7.48g为一氧化氮和二氧化氮 气体质量,消耗氢氧化钠物质的量=0.2L×1mol/L-0.1mol/L×0.2L=0.18mol;设NO物质的量为x,NO2物质的量为y,得到:
x+y=0.18
30x+46y=7.48
解得x=0.05mol,y=0.13mol
NO和NO2的物质的量之比=0.05:0.13=5:13;故答案为:5:13;
(5)如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生白烟,氨气被氧化生成一氧化氮,一氧化氮和空气中的氧气反应生成二氧化氮,通入水中反应生成硝酸,硝酸和过量的氨气反应生成硝酸铵固体小颗粒,冒白烟;反应为:4NO+3O2+2H2O=4HNO3,或2NO+O2=2NO2和3NO2+H2O=2HNO3+NO或4NO2+O2+2H2O=4HNO3;NH3+HNO3=NH4NO3,故答案为:4NO+3O2+2H2O→4HNO3,或2NO+O2→2NO2和3NO2+H2O→2HNO3+NO,或4NO2+O2+2H2O→4HNO3;NH3+HNO3→NH4NO3.
点评 本题考查了氨气实验室制备,性质验证方法,氨气的催化氧化反应,气体干燥试剂选择,产物吸收,过程反应化学方程式的书写,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 3478Se和3480Se 分别含有44和46个质子 | |
| B. | 3478Se和3480Se互为同位素 | |
| C. | 3478Se 和3480Se互为同素异形体 | |
| D. | 3478Se和3480Se都含有34个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一周期,从左到右,第一电离能逐渐增大 | |
| B. | 第一电离能越大,金属性越强 | |
| C. | 第三周期,从左到右,主族元素电负性逐渐增大 | |
| D. | 电负性越大,原子半径越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②③⑥ | C. | ②③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物可能是羧酸 | |
| B. | 该有机物可能是酯 | |
| C. | 该有机物可能含有碳碳双键 | |
| D. | 将该有机物和CH4混合,共5mol,完全燃烧,共消耗10mol O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{56b}{a}$ | B. | $\frac{b}{168a}$ | C. | $\frac{3b}{168a}$ | D. | $\frac{b}{56a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 | |
| B. | 制取并用排水法收集氧气结束后,应立即停止加热 | |
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 金属钠着火,应该立即用水扑灭 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com