
已知NCl3 在常温下是一种淡黄色的液体,遇水即发生水解:NCl3+ 3H2O = NH3 +3HClO下列说法正确的是
A、NCl3是非极性分子
B、Cl的化合价为-1价
C、非金属性:N > Cl
D、NCl3与水反应时,NCl3既是氧化剂又是还原剂
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:



 H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大 H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 ,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:

查看答案和解析>>
科目:高中化学 来源: 题型:
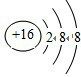

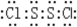
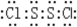
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com