
| ||
| 56L |
| 22.4L/mol |
| 42.5g |
| 17g/mol |


科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013届江苏省徐州市高三模底考试化学试卷(带解析) 题型:填空题
(14分)碳氧化物和氨氧化物在工业生产中有着广泛应用。
(1)工业上利用CO和H2在催化剂存在下合成甲醇。
主反应:CO(g)+2H2(g)=CH3OH(g) △H=-91kJ.mo1-1
副反应:2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) △H=-206 kJ.mo1-1
①反应2CH3OH(g)=CH3OCH3(g)+H2O(g)的△H= kJ.mo1-。
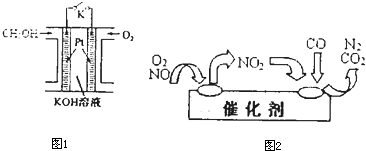
②工业中常用醇为燃料制成燃料电池(如右图所示),通入甲醇的电极是 极(填“正”或“负”);该电池的正极反应式为 。
(2)氮氧化物进入大气后,可形成硝酸型酸雨和光化学烟雾,必须对其进行处理。
①用过量的NaOH溶液吸收NO2气体,所得的溶液中除了含有NaOH,还含有 。
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如右图所示。写出净化过程中的总化学反应方程式: 。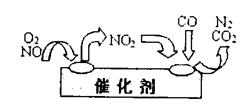
③某工厂排出的尾气中NOx的含量为0.56%(体积分数),用氨气可以将其转化为无害气体,发生的反应为:6NOx+4xNH3=(3+2x)N2+6xH2O若处理1× L(标准状况)该尾气需42.5gNH3,则x= 。
L(标准状况)该尾气需42.5gNH3,则x= 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省徐州市高三模底考试化学试卷(解析版) 题型:填空题
(14分)碳氧化物和氨氧化物在工业生产中有着广泛应用。
(1)工业上利用CO和H2在催化剂存在下合成甲醇。
主反应:CO(g)+2H2(g)=CH3OH(g) △H=-91kJ.mo1-1
副反应:2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) △H=-206 kJ.mo1-1
①反应2CH3OH(g)=CH3OCH3(g)+H2O(g)的△H= kJ.mo1-。
②工业中常用醇为燃料制成燃料电池(如右图所示),通入甲醇的电极是 极(填“正”或“负”);该电池的正极反应式为 。

(2)氮氧化物进入大气后,可形成硝酸型酸雨和光化学烟雾,必须对其进行处理。
①用过量的NaOH溶液吸收NO2气体,所得的溶液中除了含有NaOH,还含有 。
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如右图所示。写出净化过程中的总化学反应方程式: 。

③某工厂排出的尾气中NOx的含量为0.56%(体积分数),用氨气可以将其转化为无害气体,发生的反应为:6NOx+4xNH3=(3+2x)N2+6xH2O若处理1× L(标准状况)该尾气需42.5gNH3,则x=
。
L(标准状况)该尾气需42.5gNH3,则x=
。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省苏州五中高三(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com