
| A、Fe |
| B、FeO |
| C、Fe(OH)3 |
| D、FeSO4 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、1 mL 0.5 mol?L-1的NaOH溶液 |
| B、100 mL 0.01 mol?L-1的NaCl溶液 |
| C、100 mL 0.1 mol-1的NaOH溶液 |
| D、10 mL 0.1 mol?L-1的Na2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数/% | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-389.9 kJ/mol | ||
B、C2H2(g)+
| ||
| C、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)△H=-2599.2 kJ/mol | ||
| D、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-1299.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4,C2H6 |
| B、C2H4,C3H8 |
| C、C2H4,C3H6 |
| D、C2H2,C4H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 转变成
转变成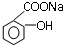 的方法是( )
的方法是( )| A、加入足量的NaOH(aq)并加热 |
| B、与足量NaOH(aq)共热后,通入足量CO2 |
| C、与盐酸共热后,加入足量的NaOH(aq) |
| D、与稀硫酸共热后,加入足量Na2CO3 (aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:


 的一种同分异构体满足下列条件:
的一种同分异构体满足下列条件: 试写出只用1,3-丁二烯合成六元环化合物的结构简式
试写出只用1,3-丁二烯合成六元环化合物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向苏打和小苏打溶液中分别加入足量稀盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| C | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
| D | 将水蒸气通过灼热的铁粉,将生产的气体通入肥皂液中,点燃肥皂泡 | 产生爆鸣声 | 铁与水在高温下发生反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com