
| A. | 氧化物 | B. | 单质 | C. | 碱 | D. | 电解质 |
分析 碱性氧化物、碱都能与酸反应生成盐和水,金属单质和酸反应生成盐和氢气或含氮气体,在水溶液里或熔融状态下能导电的化合物是电解质,可以是碱、碱性氧化物等.
解答 解:A、碱性氧化物和酸反应生成盐和水,所以A可能是氧化物,故A不选;
B、金属单质和酸反应可能生成盐和氢气,也可能生成含氮物质,如铁和过量硝酸反应生成盐、水和一氧化氮,所以A不可能是单质,故B选;
C、碱和酸发生中和反应生成盐和水,所以A可能是碱,故C不选;
D、碱及金属氧化物都属于电解质,能和酸反应生成盐和水,所以A可能是电解质,故D不选;
故选B
点评 本题根据反应类型确定反应物,明确物质的性质是解本题关键,知道哪些物质能和酸反应生成盐和水,易错选项是C,注意金属和硝酸反应的生成物特点,为易错点


科目:高中化学 来源: 题型:选择题
| A. | 用KMnO4(H+)溶液鉴别甲苯、丙烯、已烷 | |
| B. | 用溴水鉴别苯、丙烯、四氯化碳 | |
| C. | 用水鉴别乙醇、苯、四氯化碳 | |
| D. | 用NaOH溶液鉴别苯酚溶液、甲苯、硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
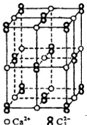 碳族元素的单质及其化合物是一类重要物质.请回答下列问题:
碳族元素的单质及其化合物是一类重要物质.请回答下列问题: ,其中碳氧原子之间共价键是c(填序号).
,其中碳氧原子之间共价键是c(填序号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||
| X | Y | Z |
| A. | X的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X>R | |
| C. | Z的单质能与Y的某些化合物发生置换反应 | |
| D. | R的最高价氧化物对应水化物分子为HRO3或H3RO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 | 有难溶物存在 |
| 步骤2: | ①有无色气泡产生,说明有CaCO3 ②出现无色气泡,说明含有碳酸钙,说明有若有难溶物存在,说明有二氧化硅 |
| 步骤3: | |
| … |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开始加入合金的总物质的量为0.15mol | |
| B. | 生成NO气体体积在标准状况下为2.24L | |
| C. | 生成沉淀完全时消耗NaOH溶液体积为100mL | |
| D. | 原硝酸物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 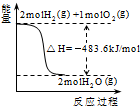 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 | |
| B. | 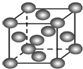 表示Cu形成金属晶体时的堆积方式 表示Cu形成金属晶体时的堆积方式 | |
| C. | 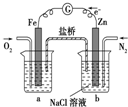 装置中烧杯a中的溶液pH降低 装置中烧杯a中的溶液pH降低 | |
| D. |  装置中待镀铁制品应与电源正极相连 装置中待镀铁制品应与电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若两种恰好中和,则一定是a=b | B. | 若混合液显碱性,则一定是b≥a | ||
| C. | 若混合液显中性,则可能有a>b | D. | 若混合液显酸性,则可能有a≤b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com