
【题目】对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是( )
A. 含氧原子的个数比为2∶3
B. 含硫元素的质量比是5∶4
C. 含氧元素的质量比为5∶4
D. 含硫原子的个数比为1∶1
【答案】B
【解析】
对于相同质量的二氧化硫和三氧化硫,假设质量都是1g,则物质的量分别是![]() mol、
mol、![]() mol,物质的量比是
mol,物质的量比是![]() :
:![]() =5:4。
=5:4。
A. 二氧化硫和三氧化硫分子物质的量比是5:4,则含氧原子的个数比为(5×2):(4×3)=5∶6,故A错误;
B. 二氧化硫和三氧化硫分子物质的量比是5:4,含硫原子物质的量比是(5×1)∶(4×1)=5:4,硫元素质量比是5:4,故B正确;
C. 二氧化硫和三氧化硫分子物质的量比是5:4,含氧原子的物质的量比为(5×2):(4×3=5∶6,氧原子的质量比为5:6,故C错误;
D. 二氧化硫和三氧化硫分子物质的量比是5:4,含硫原子的个数比为(5×1):(4×1)=5∶4,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】2020年是太原市创建第六届全国文明城市的攻坚之年,目标是努力打造宜居、宜业、宜乐、宜游的良好环境,持续提升城市文明程度和市民文明素质。下列做法不符合这一目标的是( )
A.使用可降解快餐盒
B.种植绿色无公害蔬菜
C.随意丢弃使用过的医用口罩
D.将普通灯泡更换为LED节能灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g)![]() 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
容器1 | 容器2 | 容器3 | |
反应温度T/K | 700 | 700 | 800 |
反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
平衡v正(SO2)/mol·L-1·s-1 | v1 | v2 | v3 |
平衡c(SO3)/mol·L-1 | c1 | c2 | c3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率a | a 1(SO2) | a 2(SO3) | a 3(SO2) |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是
A. v1< v2,c2< 2c1 B. K1> K3,p2> 2p3
C. v1< v3,α1(SO2 ) < α3(SO2 ) D. c2> 2c3,α2(SO3 )+α3(SO2 )<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是 ( )
A. 1 mol CO2 的质量为44 g/mol
B. 硝酸的摩尔质量63g
C. 2gH2所含原子数目为2mol
D. 0.5molNa2SO4溶于水中,所得溶液中Na+个数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol NH3气体(假设生成气体完全逸出),同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体(已知难溶性碱受热易分解,生成相应的金属氧化和水,如 M(OH)n![]() MOn/2+n/2H2O向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中 ( )
MOn/2+n/2H2O向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中 ( )
A. 至少存在3种离子
B. CO32-、K+—定不存在
C. SO42-、NH4+、Fe3+一定存在,Cl-可能不存在
D. Cl- 一定存在,且 n (Cl-) ≥0.04mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中山大学颜光美课题组发现的一种“M1”天然病毒(直径约为70nm,外壳是蛋白质)能杀伤某些癌细胞,而不伤害正常细胞。下列有关说法中,正确的是( )
A.M1中只含C、H元素
B.蛋白质属于高分子化合物
C.M1分散在水中形成的是浊液
D.蛋白质水解的最终产物是CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:

(1)碳原子价层电子的轨道表达式为__________,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______。NH3比PH3的沸点高,原因是_________。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________。
(4)EMIM+离子中,碳原子的杂化轨道类型为______。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则EMIM+离子中的大π键应表示为________。
),则EMIM+离子中的大π键应表示为________。

(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______晶体,其中硼原子的配位数为_______。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为________(列出化简后的计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将BaO2放入密闭真空容器中,反应2BaO2(s)![]() 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
A. 保持体积不变,升高温度 B. 保持温度不变,缩小容器的体积
C. 保持体积和温度不变,充入一定量的氧气 D. 保持体积和温度不变,加入BaO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图所示(未表示出原子或原子团的空间排列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是
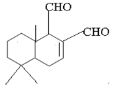
A. H2
B. Ag(NH3)2OH溶液
C. HBr
D. Br2的CCl4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com