
�軯����һ����Ҫ�Ļ�������ԭ�ϣ�ͬʱҲ��һ �־綾���ʣ�����Σ�����ཡ����һ��й¶��Ҫ��ʱ������һ�����ͨ������˫��ˮ�������������Һ���������Լ��ỷ����Ⱦ��
�־綾���ʣ�����Σ�����ཡ����һ��й¶��Ҫ��ʱ������һ�����ͨ������˫��ˮ�������������Һ���������Լ��ỷ����Ⱦ��
��֪���軯�ƻ�ѧʽΪNaCN(CԪ�أ�2�ۣ�NԪ�أ�3��)���軯����һ�ְ�ɫ�ᾧ�������綾�������� ˮ��ˮ��Һ�ʼ��ԣ���ˮ�������軯�⡣
ˮ��ˮ��Һ�ʼ��ԣ���ˮ�������軯�⡣
(1)NaCN��˫��ˮ��������һ����ʽ�κ�һ����ʹʪ���ɫʯ����ֽ���������壬�÷�Ӧ�����ӷ���ʽ�� ��
(2)�軯������������Ƶķ�ӦΪ��NaCN+Na2S2O3�TNaSCN+Na2SO3����֪��NaSCN��SΪ-2�ۣ�����1molNaCN����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ___________��
(3)CN����CԪ���ԣ�2�ۣ�NԪ���ԡ�3�ۣ���ǽ�����N__ _C(�����������������)�������ʵ��֤����_____________��
ij��ѧ��ȤС��ʵ�����Ʊ����������(Na2S2O3)��������������������Һ��������軯�Ʒ�ˮ�ܷ����ŷš�
��ʵ��һ��ʵ����ͨ����ͼװ���Ʊ�Na2S2O3��

(4)bװ�õ������� ��cװ���еIJ�����Na2S2O3��CO2�ȣ�dװ���е�������NaOH��N a2CO3���������� ��
a2CO3���������� ��
(5)ʵ���������e���������ʢ (ѡ�NaOH��Һ������ˮ������CCl4������һ��)��ע�������ٹر�K2��K1����ֹ���װ��ʱ��Ⱦ������
��ʵ������ⶨ�������������Һ������ķ�ˮ ���軯�Ƶĺ�����
���軯�Ƶĺ�����
��֪��
�ٷ�ˮ���軯�Ƶ�����ŷű�Ϊ0��50mg/L��
��Ag����2CN����[Ag(CN)2]����Ag����I����AgI����AgI�ʻ�ɫ����CN��������Ag����Ӧ��
ʵ�����£�
ȡ20��00mL��������軯�Ʒ�ˮ����ƿ�У����μӼ���KI��Һ��ָʾ������1��000��10��4mol/L�ı�AgNO3��Һ�ζ�������AgNO3��Һ�����Ϊ1��50mL��
(6)�ζ��յ���жϷ����� ��
(7)������ķ�ˮ�Ƿ�ﵽ�ŷű� (��ǡ���)��
 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡʯ��ׯ�и����ϵ�һ�νο��Ի�ѧ���������棩 ���ͣ�ѡ����
ij���ӷ�Ӧ���漰H2O��ClO-��NH4+��H+��N2��Cl-������������N2�����ʵ�����ʱ��仯��������ͼ��ʾ�������ж���ȷ����

A���÷�Ӧ�Ļ�ԭ����Cl-
B������1 mol��ԭ����ת��6 mol����
C���������뻹ԭ�������ʵ���֮��Ϊ2:3
D����Ӧ����Һ������������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹŸ�����9���¿���ѧ���������棩 ���ͣ������
ij��ѧ��ȤС��������ʯ����Ҫ�ɷ�ΪFe2O3������SiO2��A12O3�����ʣ���ȡFe2O3�������������£�

��1����I���ͣ������з�����Һ�ͳ����IJ��������� ��
��2��д��Fe2O3�����ᷴӦ�����ӷ���ʽ ��
��3������A����Ҫ���� ��
��4����ҺY�е������ӳ�OH����Cl���⣬���� ��д���ӷ��ţ���
��5�����˳���������ʱ��ϴ�ӳ�����ϴ�ӳ����ľ������Ϊ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹŸ�����9���¿���ѧ���������棩 ���ͣ�ѡ����
O2F2���Է�����Ӧ��H2S+4O2F2 = SF6+2HF+4O2������˵����ȷ���ǣ� ��
A����������������
B��O2F2�������������ǻ�ԭ��
C��������4.48 L HF����ת��0.8 mol����
D����ԭ���������������ʵ���֮��Ϊ1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹŸ�����9���¿���ѧ���������棩 ���ͣ�ѡ����
����������Ʊ�������ʵ���У�������ó��Ľ��۴�����ǣ� ��
ѡ�� | �Լ� | ��ֽ����Һ | ���� | ���� |
A | Ũ��ˮ����ʯ�� | ��ɫʯ����ֽ | ���� | NH3Ϊ�������� |
B | Ũ���ᡢŨ���� | pH��ֽ | ��� | HClΪ�������� |
C | Ũ���ᡢ�������� | ���۵⻯����Һ | ���� | Cl2���������� |
D | �������ơ����� | Ʒ����Һ | ��ɫ | SO2���л�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ�ڵڶ��ζο���ѧ�Ծ��������棩 ���ͣ�ѡ����
M��Q��R��VΪ�ֱ�ռ��ǰ3���ڵ�Ԫ�أ���ԭ�������������ӣ�M��R��Q��V����ͬһ���壬�����ǵ�����������֮��Ϊ14������˵������ȷ���ǣ� ��
A�����ʵķе㣺M>Q
B��QԪ�ص������Ӻ�VԪ�ص������Ӷ�ֻ�л�ԭ��[
C��M ��Q��R��V
��Q��R��V ����Ԫ����ɵĻ������ˮ��Һ������
����Ԫ����ɵĻ������ˮ��Һ������ ��
�� �ԡ����Ժ�����
�ԡ����Ժ�����
D��Q��R�������2�����ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ�ڵڶ��ζο���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����εĹ�������ټ���ʱ������������ڼ�ˮ�ܽ�ʱ�г������ɣ��ҳ�������ϡ���ᡣ�������������Ļ������ ( )
��BaCl2��(NH4)2SO3 ��AgNO3��NH4Cl ��FeCl3��NaHCO3 ��KCl��Na2CO3
A���ڢ� B�� �٢� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��������У����������ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й���Ԫ�ؼ��仯�����˵����������ȷ����
A����ƿ��Ʊ����ᾭ��������S SO3
SO3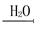 H2SO4
H2SO4
B�������������еĽ��������ﷴӦ����Ԫ���Ե��ʵ���ʽ����������
C����ȼú�м���ʯ��ʯ�ɼ���SO2�ŷţ������ķ�ӦΪ
2CaCO3��2SO2��O2===2CO2��2CaSO4
D�������е���п��(ZnS)��������ͭ��Һת��Ϊͭ��(CuS)��˵��CuS���ȶ��������л�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡʵ�������ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ʵ����
ClO2�ڳ�������һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ��59�棬�е�Ϊ11.0�棬������ˮ����ҵ�����Գ�ʪ��KClO3�Ͳ��ᣨH2C2O4����60��ʱ��Ӧ�Ƶá�ijѧ������ͼ1��ʾװ��ģ�ҵ��ȡ���ռ�ClO2��


ͼ1 ͼ2
��1��Aװ�õ綯������������� ��Aװ�ñ��������¶ȿ���װ�ã����ƾ����⣬����Ҫ�IJ����������ձ��� ��
��2��Bװ�ñ�����ڱ�ˮԡ�У���ԭ���� ��
��3����Ӧ����װ��C�пɵ�NaClO2��Һ��
��֪��.NaClO2������Һ���¶ȵ���38��ʱ����������NaClO2��3H2O�����¶ȸ���38��ʱ����������NaClO2���¶ȸ���60��ʱNaClO2�ֽ�����NaClO3��NaCl��
��.NaClO2���ܽ��������ͼ2��ʾ���벹���NaClO2��Һ���Ƶ�NaClO2����IJ������裺
�ټ�ѹ��55�������ᾧ���� ���� ���� ���õ���Ʒ��
��4��ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10.00 mL��ϡ�ͳ�100.00 mL��������ȡV1 mL�������뵽��ƿ�У�
����2����ϡ�������������pH��2.0������������KI���壬����Ƭ�̣�
����3������ָʾ������c mol��L-1 Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2 mL����֪2 Na2S2O3 + I2 ��Na2S4O6 + 2NaI����
����100 mL c mol��L-1 Na2S2O3����Һʱ���õ��IJ����������ձ�����Ͳ����������У� ��
�ڵζ������н�������ƽ�вⶨ��ԭ���� ��
��ԭClO2��Һ��Ũ��Ϊ g��L-1���ú���ĸ����ʽ��ʾ����
�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ��� �����ƫ�ߡ�����ƫ�͡����䡱 ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com