
【题目】![]() 与稀盐酸反应生成
与稀盐酸反应生成![]() 的量与反应时间的关系如图所示。下列结论中不正确的是
的量与反应时间的关系如图所示。下列结论中不正确的是![]()
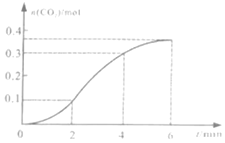
A.反应在![]() min内生成
min内生成![]() 的平均反应速率为
的平均反应速率为![]()
![]()
B.反应开始4min内,温度变化比浓度变化对反应速率的影响更大
C.4min后,反应速率减小的主要原因是![]() 减小
减小
D.图中反应在![]() 内的平均反应速率最小
内的平均反应速率最小
【答案】A
【解析】
![]() 与稀盐酸的反应为放热反应,随着反应的进行,温度逐渐升高,盐酸浓度逐渐降低,结合各时间段二氧化碳物质的量的变化可比较反应速率的大小,以此解答该题。
与稀盐酸的反应为放热反应,随着反应的进行,温度逐渐升高,盐酸浓度逐渐降低,结合各时间段二氧化碳物质的量的变化可比较反应速率的大小,以此解答该题。
A.由图可知![]() 内生成二氧化碳
内生成二氧化碳![]() ,但体积未知,不能确定反应速率,故A错误;
,但体积未知,不能确定反应速率,故A错误;
B.由图象可知,反应刚开始时反应速率较小,然后逐渐增大,因该反应为放热反应,则温度升高,开始4min内温度对反应速率的影响比浓度大,故B正确;
C.随反应进行氢离子浓度降低,氢离子浓度变化使反应速率降低,由图象可知,![]() 反应刚开始,温度较低此时反应速率由氢离子浓度决定,
反应刚开始,温度较低此时反应速率由氢离子浓度决定,![]() 反应速率最快,
反应速率最快,![]() 温度对反应速率起主要作用,4min后反应速率又降低,氢离子浓度起主要作用,故C正确;
温度对反应速率起主要作用,4min后反应速率又降低,氢离子浓度起主要作用,故C正确;
D.由图可知图中反应在![]() 内曲线斜率最小,则平均反应速率最小,故D正确;
内曲线斜率最小,则平均反应速率最小,故D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】11、浓度均为 ![]() 的
的![]() 和
和 ![]() ,在一定条件下发生反应
,在一定条件下发生反应![]()
![]()
![]() ,测得
,测得![]() 的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
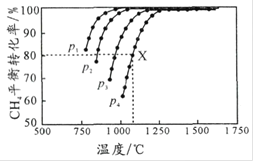
A.平衡时CO与![]() 的物质的量比为
的物质的量比为![]()
B.![]() 由大到小的顺序为
由大到小的顺序为 ![]()
C.![]() , p
, p![]() 条件下,该反应
条件下,该反应![]() 时达到平衡点X,则
时达到平衡点X,则 ![]()
D.随着温度升高,该反应的平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热。下列说法中,正确的是

A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎纸条的作用是固定小烧杯
D. 若将盐酸体积改为60 mL,理论上所求中和热不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙醇进料量(单位:mL·min-1)的关系如图所示(保持其他条件相同)。
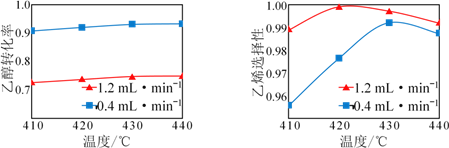
在410~440℃温度范围内,下列说法不正确的是
A. 温度一定时,随乙醇进料量增大,乙醇转化率减小
B. 温度一定时,随乙醇进料量增大,乙烯选择性增大
C. 乙醇进料量一定时,随温度的升高,乙烯选择性一定增大
D. 选择适当的催化剂在一定条件下,可大幅提高乙烯在最终产物中的比率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒压密闭容器M(如图Ⅰ)和恒温恒容密闭容器N(如图Ⅱ)中,两容器中均加入a molA和a molB,起始时两容器体积均为VL,发生如下反应并达到化学平衡状态:2A(?)+ B(?)![]() xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是
xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是

A. x=2
B. 若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态
C. A为气体,B为非气体,则平衡时M、N中C的物质的量相等
D. 若A、B均为气体,平衡时M中A的转化率小于N中A的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是( )

A. 图1可能表示压强对可逆反应A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
B. 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
C. 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH到4左右
D. 当反应COCl2(g) ![]() CO(g) + Cl2(g) △H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
CO(g) + Cl2(g) △H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。
(一)CO2的化学捕获:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___(写含碳粒子符号)。(室温下,H2CO3的Ka1=4.3×10﹣7;Ka2=5.6×10﹣11)
(2)固体氧化物电解池(SOEC)用于高温共电解CO/H2,既可实现CO2的减排又可高效制备合成气(CO/H2),其工作原理如图。写出电极A发生的电极反应式___。
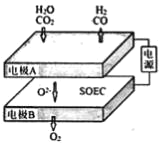
(二)CO2的综合利用
(1)CO2与CH4经催化重整制得合成气:
反应Ⅰ.CH4(g)H+CO2(g)2CO(g)+2H2(g)△H1
已知氢气、一氧化碳和甲烷的标准燃烧热(25℃)如表所示
物质 | H2(g) | CO(g) | CH4(g) |
标准燃烧热△H/kJmol﹣1 | ﹣285.8 | ﹣283.0 | ﹣890.3 |
则反应I的△H=___kJmol﹣1。
(2)用CO2催化加氢制取二甲醚的反应为:反应Ⅱ.2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g),在10L恒容密闭容器中,均充入2mol CO2和6moH2,分别以铱(Ir)和铈(Ce)作催化剂,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图1。
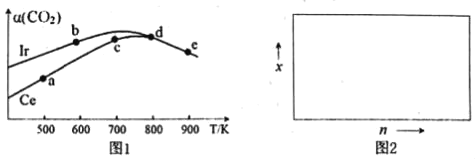
①根据图1,下列说法不正确的是___。
A.反应Ⅱ的△H<0,△S<0
B.用Ir和Ce作催化剂时,反应Ⅱ的活化能更低的是Ce
C.状态d时,v(正)<v(逆)
D.从状态b到d,α(CO2)先增大后减小,减小的原因可能是温度升高平衡逆向移动
②状态e(900K)时,α(CO2)=50%,则此时的平衡常数K=___。
③若H2和CO2的物质的量之比为n:1,900K时相应平衡体系中二甲醚的物质的量分数为x,请在图2中绘制x随n变化的示意图。_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:

下列说法错误的是( )
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B.若反应①通过原电池来实现,则ClO2是正极产物
C.反应②中的H2O2可用NaClO4代替
D.反应②条件下,ClO2的氧化性大于H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2l恒温恒容容器中加入2molMgSO4并充入 2molCO,发生反应:MgSO4(s)+ CO(g)![]() MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是

A. 0 ~2min内平均反应速率v(SO2)= 0.3 mol·l-1 ·min-1
B. 2 ~4min内容器内气体的密度没有变化
C. 该温度下,反应的平衡常数为1.8
D. 保持其他条件不变,起始时向容器中充入1.00 mol MgSO4和1.00 molCO,反应达到平衡时,n(CO2)> 0.60 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com