
请按要求回答下列问题:
(1)新出土的青铜器若保存不善,在潮湿的环境中容易生成铜绿,该腐蚀过程中的负极反应式为:_________________________。
(2)惰性电极电解饱和Na2S溶液时,在阳极附近没有看到预期的浑浊现象,探究发现,其生成了Na2Sx,则阳极反应式为:_____________________。当阳极产生1mol Sx2-时,阴极产生的气体在标准状况下的体积为_________L。(用含x的代数式表示)
(3)合成氨工业中,天然气能代替煤用于生产原料气——H2,且反应类似。请写出天然气转化为H2的两步反应方程式:______________________________________,
___________________________________________。
(4)已知:
|
酸 |
电离常数(Ka) |
酸 |
电离常数(Ka) |
|
CH3COOH |
1.8×10-5 |
HCN |
5×10-10 |
|
H2CO3 |
Ka1 = 4.2×10-7 |
HClO |
3×10-8 |
|
Ka2 = 5.6×10-11 |
①上述四种酸中,酸性最强的是 ;
②25℃时,0.01 mol/L NaCN溶液的pH________7;
③在浓度均为0.01 mol/L的CH3COONa、NaClO、Na2CO3的混合溶液中,逐滴加入0.01 mol/L HCl,则体系中酸根离子反应的先后顺序为 ;
④25℃时,向20mL 0.1 mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图像正确的是_____________。


A B


C D
(18分)
(1) Cu - 2e— = Cu2+ (2分)
(2) xS2- - (2x-2) e— = Sx2- ; 22.4(x-1) (各2分)
(3) CH4 + H2O =" CO" + 3H2; CO + H2O = CO2 + H2(各2分)
(4)①CH3COOH;② > ;(各1分)
③CO32—、ClO—、HCO3—、CH3COO—(4分)
④C(2分)
【解析】
试题分析:(1)铜作为负极失去电子,电极式为:Cu - 2e— = Cu2+。(2)阳极失去电子,发生的是氧化反应,元素的化合价升高,因此电极式为:xS2- - (2x-2) e— = Sx2- ,阳极产生1mol Sx2-时,转移电子数为(2x-2) mol,根据2H++ 2e—=H2↑,计算生成气体的体积为:22.4(x-1)L。(4)电离常数越大,其酸性越强;反之则弱。
考点:电解原理弱电解质的电离平衡
点评:本题考查的是电解原理和弱电解质的电离平衡的相关知识,学生要对其原理分析透彻,并利用好题中所给出的信息。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:

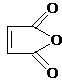
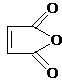
| 浓H2SO4 |
| △ |
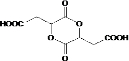
| 浓H2SO4 |
| △ |

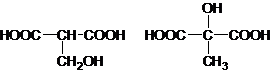
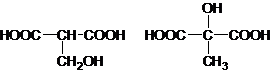
查看答案和解析>>
科目:高中化学 来源: 题型:
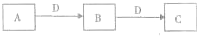
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
族 周期 |
ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||




查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com