
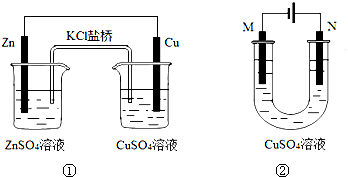
| A、装置①中盐桥内的K+移向CuSO4溶液 |
| B、装置①将电能转变为化学能 |
| C、若装置②用于铁棒镀铜,则N极为铁棒 |
| D、若装置②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
| A、自然界中没有游离态的硅,纯净的硅晶体可用于制作光导纤维 |
| B、可用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 |
| C、钢材是合金,合金的熔点低,硬度大 |
| D、用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
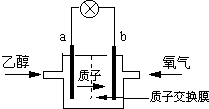 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A、a极为电池的正极 |
| B、电池工作时电流由a极沿导线经灯泡再到b极 |
| C、电池负极的电极反应为:4H++O2+4e-=2H2O |
| D、电池工作时,1mol乙醇被氧化时就有12mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与乙醇反应时,NH5被氧化 |
| B、NH5中N元素的化合价为+5价 |
| C、1 mol NH5中含有5 molN-H键 |
| D、1 mol NH5与H2O完全反应,转移电子2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | T | X | Y | Z | W |
| 原子半径/nm | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
| A、X的阴离子半径小于T的阳离子半径 |
| B、Y的氢化物的热稳定性比Z的氢化物的大 |
| C、Y单质与Fe反应生成的化合物中,铁元素显+3价 |
| D、Z元素的氧化物对应的水化物一定为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol苯分子含有3NA个C-C键 |
| B、一定条件下,1mol N2和3mol H2充分混合,反应后转移的电子数为6NA |
| C、常温下,78.0g Na2O2与58.5g NaCl所含阴离子数相等 |
| D、标准状况下,2.24L CCl4所含分子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com