
【题目】分子式C4H8O2的有机物与硫酸溶液共热可得有机物A和B.将A氧化最终可得C,且B和C为同系物.若C可发生银镜反应,则原有机物的结构简式为( )
A.HCOOCH2CH2CH3
B.CH3COOCH2CH3
C.CH3CH2COOCH3
D.HCOOCH(CH3)2
科目:高中化学 来源: 题型:
【题目】氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取。反应原理、实验装置图(加热装置都已略去)如下: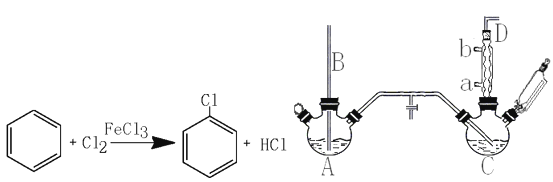
已知:氯苯为无色液体,沸点132.2℃,常温下不与氢氧化钠溶液反应。
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是。冷凝管中冷水应从(填“a”或“b”)处通入。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯。
①对C加热的方法是(填序号)。
a.酒精灯加热 b.酒精喷灯加热 c.水浴加热
②D出口的气体成分有HCl、和。
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本。写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:;(写两个即可)。
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是。
(5)工业生产中苯的流失情况如下:
项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
则1t苯可制得成品为t(只要求列式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去). A ![]() B
B ![]() C
C ![]() D
D
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体. ①D的化学式是;
②在工业生产中,B气体的大量排放被雨水吸收后形成了而污染了环境.
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 , 用化学方程式表示该物质与水的反应 . 将C长期露置于空气中,最后将变成物质D,D的化学式为 . 现在有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .
(3)若C是红棕色气体.图是实验室制取A气体的装置: 
①写出实验室制取A的化学方程式 .
②为了检验氨气是否集满,可将 , 则证明已收集满.D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.淀粉和纤维素都可以在酸性条件下水解生成葡萄糖
B.煤的气化、液化和干馏都是煤综合利用的主要方法,都属于物理变化
C.地沟油发生皂化反应后加入饱和食盐水,搅拌发现液面上有固体物质
D.蛋白质溶液中加入浓的硫酸铵溶液,有固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.活化分子间的碰撞一定能发生化学反应
B.升高温度时,化学反应速率加快,主要原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.自发进行的反应一定迅速
D.凡是熵增加的过程都是自发过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两位学生想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6molL﹣1H2SO4溶液中,乙同学将电极放入6molL﹣1的NaOH溶液中,如图所示. 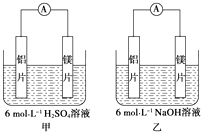
(1)如果甲、乙同学均认为若构成原电池的电极材料都是金属,则构成负极材料的金属应比构成正极材料的金属活泼,则甲会判断出的活动性更强,而乙会判断出的活动性更强(填元素符号).
(2)由此实验,可得到哪些正确的结论?(填字母).
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,已没有实用价值
D.该实验说明化学研究的对象复杂,反应受条件影响较大,因此应具体问题具体分析
(3)上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池的正、负极”的做法(填“可靠”或“不可靠”).如不可靠,请你提出另一个判断原电池正、负极的可行的实验方案(如可靠,此空可不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表(律)说法正确的是
A. 最外层有两个电子的原子一定在ⅡA 族
B. IA族均为碱金属
C. 同一周期核电荷数越大原子半径越大
D. 同一主族核电荷数越大元素金属性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其元素特征信息如下表.回答下列问题:
元素编号 | 元素特征信息 |
A | 是原子半径最小的元素 |
B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
C | 是短周期元素中原子半径最大的主族元素. |
D | 其氢氧化物和氧化物都有两性,与C同周期 |
E | 与C同周期,原子半径在该周期最小 |
F | 原子有三个电子层,且最外层电子数是最内层电子数的3倍, |
(1)写出下列元素的符号:B: , E:;
(2)写出C与B 形成的两种离子化合物的化学式; .
(3)写出B与A 形成的两种化合物的电子式; .
(4)含B、C、F 三种元素的化合物有、(请填写具体的化学式,至少2种).
(5)D单质和C的最高价氧化物对应水化物水溶液反应的离子方程式: .
(6)FB2和E元素的单质在水溶液中反应的化学方程式是 .
(7)D的单质和氧化铁反应可用于野外焊接钢轨,该反应属于(填“吸热”或“放热”)反应,写出反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L密闭容器中投入一定量的A,B发生反应:3A(g)+bB (g)cC(g)△H=﹣Q kJmol﹣1(Q>0).12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示.下列说法正确的是( ) 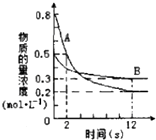
A.前12s内,A的平均反应速率为0.025molL﹣1s﹣1
B.12s后,A的消耗速率等于B的生成速率
C.化学计量数之比b:c=1:2
D.12s内,A和B反应放出的热量为0.2Q kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com