
ij�ռ���Ʒ�к����������������õĿ��������ʣ�Ϊ�˲ⶨ�䴿�ȣ��������µζ�������
A����250mL����ƿ�ж��ݳ�250mL�ռ���Һ��
B���ü�ʽ�ζ�����ȡ25mL�ռ���Һ����ƿ�в��μӼ��μ�����ָʾ����
C������ƽ��ȷ��ȡ�ռ���Ʒmg�����ձ��м�����ˮ�ܽ⣻
D�������ʵ���Ũ��ΪC mol·L-1�ı�H2SO4��Һװ����ʽ�ζ��ܣ�����Һ�棬���¿�ʼ�̶�ΪV1mL��
E������ƿ�µ�һ�Ű�ֽ���ζ����յ㣬��¼�յ�̶�ΪV2 mL��
�ش��������⣺
��1����ȷ���������˳����(����ĸ��д) 

 D
D  ��
��
��2������E�е���ƿ�µ�һ�Ű�ֽ�������� ��
��3������D��Һ��Ӧ������ ��
��4���ζ��յ�������� ��
��5������ʽ�ζ���û���ñ�H2SO4��ϴ����Բⶨ����к�Ӱ��? (�ƫ�ߡ�����ƫ�͡�����Ӱ�족��������������ȷ)��
��6�����ռ���Ʒ�Ĵ��ȼ���ʽ�� ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�ȥ���ʵIJ����У����ܴﵽĿ�ĵ���(����)
A����ȥ���е������壺����NaOH��Һ���Һ
B����ȥ�����е�������ϩ��ͨ����ˮ��ϴ��
C����ȥCO2�е�����HCl���壺ͨ��ʢ�б���NaHCO3��Һ��ϴ��ƿ
D����ȥFeCl2��Һ�е�����FeCl3����������ͭ�ۺ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��5.6g����������ϡ�����У��ټ�������������������Һ����ַ�Ӧ�����ˣ��ڿ����м����������������յ��������ٱ仯����ʱ���������Ϊ
A��7.2g B��8.0g C��9.0g D��10.7g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ͼ�жϣ�����������ȷ����
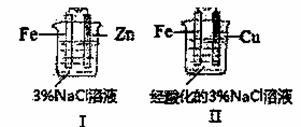
A��I�͢���������������
B��I�͢��и�����Ӧ����Fe-2e-==Fe2+
C��I�͢���������Ӧ����O2+2H2O+4e-==4OH-
D��I�͢��зֱ��������K3[Fe(CN)6]��Һ��������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ��������ܱ������з���3 L����R��5 L����Q����һ�������·�����Ӧ��2R(g)+5Q(g) 4X(g)+nY(g)����Ӧ��ȫ�������¶Ȳ��䣬��������ѹǿ��ԭ����87��5������ѧ����ʽ�е�nֵ��
4X(g)+nY(g)����Ӧ��ȫ�������¶Ȳ��䣬��������ѹǿ��ԭ����87��5������ѧ����ʽ�е�nֵ��
A��2 B��3 C��4 D��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����֧�ֱ�ʢ����ɫ��Һ���Թܣ��������²�����������ȷ����
| ���� | ���� | ���� | |
| A | �μ���ˮ��CCl4�������� | �²���Һ���Ϻ�ɫ | ԭ��Һ����I- |
| B | �μ�BaCl2��Һ | ���ɰ�ɫ���� | ԭ��Һ��һ����SO42- |
| C | �ò�˿պȡ��Һ������ɫ��Ӧ | ����ʻ�ɫ | ԭ��Һ����Na+����K+ |
| D | �μ�ϡNaOH��Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿ� | ��ֽ������ | ԭ��Һ��һ����NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڹ�����ռ����Ҫ��λ��
��1���ϳɰ���ҵ�У��ϳ�����ÿ����2 mol NH3���ų�92.2 kJ������
�� ��ҵ�ϳɰ����Ȼ�ѧ����ʽ�� ��
�� ����ʼʱ�������ڷ���2 mol N2��6 mol H2����ƽ���ų�������ΪQ����
Q���>������<����=����_______184.4 kJ��
�� ��֪��

1 mol N-H���������յ�����Լ����_______kJ��
| T / �� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
��2����ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]����Ӧ�Ļ�ѧ����ʽΪ��2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
���ʱ䦤H���>������<����=���� 0
����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�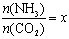 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
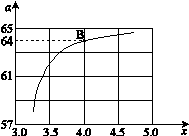 �� ��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ_______��
�� ��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ_______��
��3���������Ʊ������������һ����Ҫ���ʣ������Ļ�������;�㷺��
 ���������õ����Ʊ������������һ��;����
���������õ����Ʊ������������һ��;����
�ٹ��̢�Ļ�ѧ����ʽ��
������ʱ���Ͻ�NH3��±�أ���Cl2����װ���䡣�����߽Ӵ�ʱ���ҷ�Ӧ�������̣�����0.4 mol NH3�μӷ�Ӧʱ��0.3 mol ����ת�ơ�д����Ӧ�Ļ�ѧ����ʽ
�۰���һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϡ�
��֪��4NH3(g) + 3O2(g) == 2N2(g) + 6H2O(g) ��H = ��1316 kJ/mol�����ȼ�ϵ�صĸ�����Ӧʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ����д��ȷ���ǡ�������..��������������..��������.��..( )
A��ʵ�����ô���ʯ��ϡ������ȡCO2��2H+ + CO32- �� CO2��+ H2O
B������ϡ���ᷴӦ��Fe + 2H+ �� H 2��+ Fe 2+
C����AlCl3��Һ�м��������NaOH��Һ��Al3+ + 3OH- �� Al(OH)3��
D��NaHCO3��Һ��NaOH��Һ��Ӧ�� OH- + HCO3- �� CO32- + H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����1��Zn��s��+ 1/2O2��g����ZnO(s) ����H��-350 kJ��mol-1 ��
��2��2Ag(s) + 1/2O2��g����Ag2O(s) ����H�� -25 kJ��mol-1 ��
��Zn��s��+ Ag2O(s)��ZnO(s)+ 2Ag(s)�Ħ�H����
A��-375 kJ��mol-1 B��-325 kJ��mol-1 C��+375 kJ��mol-1 D��+325 kJ��mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com