
【题目】甲同学给分子式为C12H26的某烷烃命名为“2,4-二甲基-3,5-二乙基己烷”,乙同学认为甲同学命名错误,有关该烷烃的说法,你认为正确的是( )
A.该烷烃正确名称应为:4,5-二甲基-3-异丙基已烷
B.该烷烃分子中含有5个支链
C.该烷烃的一氯代物有11种
D.该烷烃可以看做是11种不同类型的单烯烃与氢气加成后的产物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B.二氯甲烷有两种结构
C.0.1 mol的烃能被标准状况下4.48 L H2加成,则此烃一定含有碳碳三键
D.甲苯能使酸性高锰酸钾褪色,而甲烷不能,这是因为基团间的相互影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种直接铁燃料电池(电池反应为3Fe+2O2=Fe3O4)的装置如图所示,下列说法正确的是( )
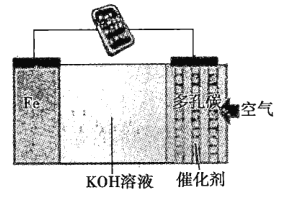
A.Fe极为电池正极
B.KOH溶液为电池的电解质溶液
C.电子由多孔碳极沿导线移向Fe极
D.5.6gFe参与反应,导线中转移1.204×1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯具有类似茉莉花香的气味,可以用甲苯和乙醇进行人工合成,其合成路线如图:
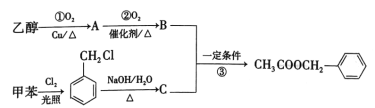
(1)写出反应①的化学方程式:___。
(2)反应③的反应类型为___。
(3)反应__(填序号)的原子利用率为100%,符合绿色化学的要求。
(4)C的结构简式为__,试写出C的另外两种不同类别的芳香类同分异构体的结构简式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是__________。
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是__________。
(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
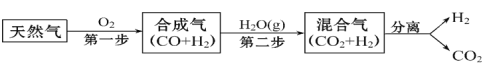
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式 ___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,某科研小组设计如下工艺流程回收铜并制取胆矾(流程中RH为萃取剂),下列说法正确的是
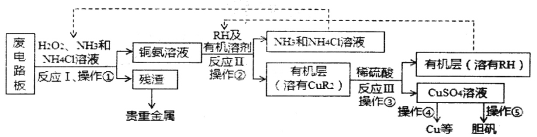
A.反应I的离子方程式为:Cu+H2O+2NH3+2NH4+==Cu(NH3)42++2H2O
B.操作②用到的主要仪器为蒸馏烧瓶
C.操作④以石墨为电极电解硫酸铜溶液:阳极产物为O2和H2SO4
D.操作⑤为:蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在现代生产和生活中发挥重要作用。
(1)可以通过热化学循环在较低温度下由硫化氢分解制备氢气。
SO2(g)+I2(s)+2H2O(1)==2HI(aq)+H2SO4(aq) △H1=—151.5kJ·mol-1
2HI(aq)==H2(g)+I2(s) △H2=+110kJ·mol-1
H2S(g)+H2SO4(aq)==S(s)+SO2(g)+2H2O(I) △H3=+65kJ·mol-1
热化学硫碘循环硫化氢分解联产氢气、硫磺的热化学方程式为_________________。
(2)硫酸厂尾气中含有大量SO2,为提高其利用率可用图1所示装置(电极均为惰性电极)将其吸收,而锂—磺酰氯(Li—SO2C12)电池可作为电源电解制备Ni(H2PO2)2(图2)。已知电池反应为:2Li+SO2C12=2LiCl+SO2↑
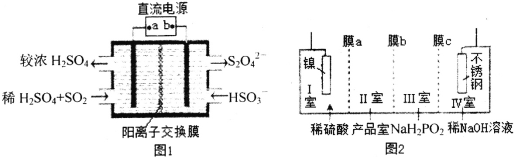
①图1中:a为直流电源的______极(填“负”或“正”),其阴极的电极反应式为_____。
②SO2C12分子中S原子的杂化方式为____________________。
③锂—磺酰氯电池的正极反应式为_______________________。
④图2中膜a为______交换膜(填“阳离子”或“阴离子”下同),膜c为_________交换膜。不锈钢电极的电极反应式为_______________________________。
(3)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g) ![]() 2SO3(g)。
2SO3(g)。
已知:标准平衡常数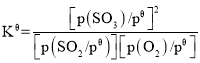 ,其中
,其中![]() 为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为
为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为![]() ,则
,则![]() _______(用含
_______(用含![]() 的最简式表示)。
的最简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,结构如图所示.下列关于该有机物的说法有如下几种:
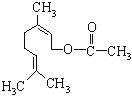
①该有机物有一种同分异构体属于酚类;
②该有机物属于酯类;
③该有机物不能发生银镜反应;
④该有机物的分子式为C11H18O2;
⑤1mol该有机物最多能与1mol NaOH反应
其中正确的是
A.①③④B.②③⑤C.①④⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中![]() 下列分析正确的是
下列分析正确的是![]()
![]()

A. ![]() 闭合,铁棒上发生的反应为
闭合,铁棒上发生的反应为![]()
B. ![]() 闭合,石墨棒周围溶液pH逐渐降低
闭合,石墨棒周围溶液pH逐渐降低
C. ![]() 闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
D. ![]() 闭合,电路中通过
闭合,电路中通过![]() 个电子时,两极共产生
个电子时,两极共产生![]() 气体
气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com