
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1的NaI溶液:K+、H+、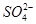 、
、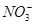
B.0.1 mol·L-1的NaHCO3溶液:K+、Na+、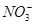 、Cl-
、Cl-
C.0.1 mol·L-1 FeCl3溶液:K+、Na+、ClO-、Cl-
D.0.1 mol·L-1的氨水:Cu2+、Na+、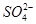 、
、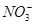
科目:高中化学 来源:2014高考名师推荐化学选做题练习2(解析版) 题型:填空题
请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 I1 I2 I3 I4 … |
In/kJ.mol-1 578 1817 2745 11578 … |
则该元素是 (填写元素符号)。
(2)基态锗(Ge)原子的电子排布式是 ,Ge的最高价氯化物分子式是 ,该元素可能的性质或应用有 ;
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物 ,下列叙述正确的有
,下列叙述正确的有
A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键
D.该分子在水中的溶解度大于2-丁烯
(4)NaF的熔点  的熔点(填>、=或<),其原因是 。
的熔点(填>、=或<),其原因是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式的书写及正误判断(解析版) 题型:选择题
下列离子方程式或化学方程式与所述事实相符且正确的是
A.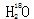 中投入Na2O2固体:
中投入Na2O2固体: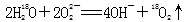
B.向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH- =H2O
C.以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O=2Cu+O2↑+4H+
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使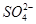 完全沉淀:Al3++2
完全沉淀:Al3++2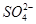 +2Ba2++4OH-=
+2Ba2++4OH-=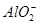 +2BaSO4↓+2H2O
+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子大量共存与推断(解析版) 题型:选择题
在水溶液中能大量共存的一组离子是
A.Fe2+、Al3+、ClO—、Cl— B.K+、Cu2+、OH、NO3—
C.NH4+、Na+、Br—、SO42— D.Mg2+、H+、SiO32-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子共存(解析版) 题型:选择题
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1 mol·L-1时有气体产生;而当溶液中c(H+)=10-13mol·L-1时又能生成沉淀。则该组离子可能是
A.Na+、Ba2+、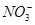 、
、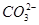
B.Ba2+、K+、Cl-、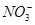
C.Mg2+、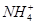 、
、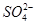 、Cl-
、Cl-
D.Fe2+、Na+、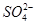 、
、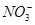
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学碳及其化合物主要性质(解析版) 题型:选择题
将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如下图所示,图中AB段表示的离子方程式先后顺序正确的是

①CO2+OH-=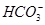 ②CO2+2OH-=
②CO2+2OH-=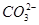 +H2O
+H2O
③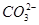 +Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2
+Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2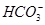
⑤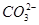 +CO2+H2O=2
+CO2+H2O=2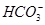
A.③① B.②⑤ C.⑤④ D.④②
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学硅及其化合物主要性质、材料(解析版) 题型:选择题
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是
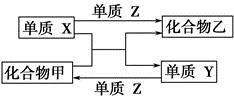
选项 | X | Y | Z | 甲 | 乙 |
A | H2 | Si | Cl2 | SiCl4 | HCl |
B | Mg | C | O2 | CO2 | MgO |
C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
D | Cl2 | N2 | H2 | NH3 | HCl |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学盐类水解的概念与离子浓度大小比较(解析版) 题型:选择题
下列反应不属于水解反应或水解方程式不正确的是
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液:HCO3-+H2O=CO32-+H3O+
⑤NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
A.①②③④ B.①②③
C.②③⑤ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com