
25℃时,将一定浓度的盐酸和一定浓度的氨水按2∶1 的体积比混合,若混合溶液中c(NH )=c(Cl-),则溶液的pH
)=c(Cl-),则溶液的pH
A.大于7 B.小于7 C.等于7 D.无法确定
科目:高中化学 来源: 题型:
将100 mL 0.30 mol·L-1的Na2SO4溶液和50 mL 0.20 mol·L-1的Al2(SO4)3溶液混合后,所得溶液中SO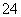 的物质的量浓度为( )
的物质的量浓度为( )
A.0.20 mol·L-1 B.0.25 mol·L-1
C.0.40 mol·L-1 D.0.50 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿佛加德罗常数,下列叙述中正确的是
A.常温常压下,22.4 L的氧气含氧原子数为2NA
B.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA
C.常温下,23g NO2含有NA个氧原子
D.足量铜与1L 18mol·L-1浓硫酸反应可以得到SO2的分子总数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。(已知:AlN+NaOH+H2O=NaAlO2+NH3↑)
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是______________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置气密性;再加入实验药品。接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是______________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见_________。
【方案2】用右图装置测定m g样品中A1N的纯度(部分夹持装置已略去)。
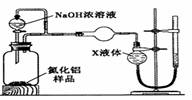
(4)为测定生成气体的体积,量气装置中的X液体可以是____________。
a.CCl4 b.H2O c.NH4Cl溶液 d.
(5)实验结束时,读取量气装置中的X液体的体积时应注意的问题有
; ; 。
【方案3】按以下步骤测定样品中A1N的纯度:
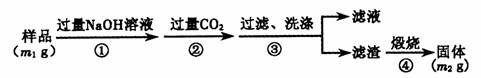
(6)样品中A1N的质量分数为 (用含m1 m2的代数式表示)。
(7)若在步骤③中未洗涤,测定结果将__________(填“偏高”、“偏低”或
“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池负极反应为:
A.H2+2OH-=2H2O+2e- B.O2+4H++4e-=2H2O
C.H2 -2e-=2H+ D.O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论正确的是
A.Pb 为正极被氧化
B.溶液的pH不断减小
C.放电时负极反应式是PbO2 +4H++ SO42-+2e-= PbSO4 +2H2O
D.溶液pH不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,在20 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是
 A. 在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
A. 在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.在B点:c(OH-)=c(H+),c(Na+)= c(CH3COO-))
C. 在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.在C点: c(CH3COO-)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是
A.已知2H2(g)+O2(g) = 2H2O(g) ΔH= - 483.6 kJ·mol-1,则氢气的燃烧热为241.8kJ·mol-1
B.已知C(石墨,s)= C(金刚石,s) ΔH=+1.9kJ·mol-1,则金刚石比石墨稳定
C.含0.5mol NaOH的稀溶液与稀醋酸完全中和,放出26.7kJ的热量,则表示该反应中和热的热化学方程式为:OH-(aq) +H+(aq)= H2O(l) ΔH
+H+(aq)= H2O(l) ΔH =-53.4kJ·mol-1
=-53.4kJ·mol-1
D.已知2H2S(g)+ O2(g)= 2S(g)+2H2O(l) ΔH1 ;
2H2S(g )+ 3O2(g)=2SO2(g)+2H2O(l)ΔH2,则ΔH1>ΔH2
)+ 3O2(g)=2SO2(g)+2H2O(l)ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述不正确的是
A.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多
B.两种溶液的物质的量浓度不相同
C.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)
D.它们分别与足量CaCO3反应时,放出的CO2一样多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com