
һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C(s)+CO2(g) 2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�����ѹ(P��)=������ѹ(P��)���������������˵����ȷ����( )
2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�����ѹ(P��)=������ѹ(P��)���������������˵����ȷ����( )
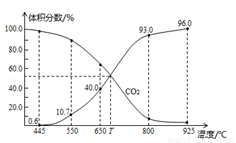
A��550��ʱ��������������壬v����v�����С��ƽ�ⲻ�ƶ�
B��650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0%
C��T��ʱ��������������CO2��CO��ƽ�����淴Ӧ�����ƶ�
D��925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=24.0P��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016��ȫ����ͨ�ߵ�ѧУ����ͳһ���Ի�ѧ���Ϻ����ο��棩 ���ͣ������
���ſ�ѧ�����ķ�չ�ͻ���Ҫ��IJ�����ߣ�CO2�IJ������ü�����Ϊ�о����ص㡣
���������գ�
��1��Ŀǰ���ʿռ�վ����CO2��һ����Ҫ�����ǽ�CO2��ԭ�����漰�ķ�Ӧ����ʽΪ��
CO2��g��+4H2��g��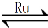 CH4��g��+2H2O��g��
CH4��g��+2H2O��g��
��֪H2������������¶ȵ����߶����ӡ�
���¶ȴ�300������400�棬���´ﵽƽ�⣬�ж����б����и��������ı仯����ѡ���������С�����䡱��
v�� | v�� | ƽ�ⳣ��K | ת���ʦ� |
��2����ͬ�¶�ʱ��������Ӧ�ڲ�ͬ��ʼŨ���·ֱ�ﵽƽ�⣬�����ʵ�ƽ��Ũ�����±���
[CO2]/mol��L-1 | [H2]/mol��L-1 | [CH4]/mol��L-1 | [H2O]/mol��L-1 | |
ƽ��� | a | b | c | d |
ƽ��� | m | n | x | y |
a��b��c��d��m��n��x��y֮��Ĺ�ϵʽΪ_________��
��3��̼�H2CO3��Ki1=4.3��10-7��Ki2=5.6��10-11
���H2C2O4��Ki1=5.9��10-2��Ki2=6.4��10-5
0.1 mol/L Na2CO3��Һ��pH____________0.1 mol/L Na2C2O4��Һ��pH����ѡ����ڡ���С�ڡ����ڡ���
��Ũ�ȹ㶫������Һ��̼����Һ�У�������Ũ�Ƚϴ����___________��
������Ũ�ȵIJ�����Һ��̼����Һ�������ϣ���Һ�и�������Ũ�ȴ�С��˳����ȷ����_____����ѡ���ţ�
a��[H+]��[HC2O4-]��[HCO3-]��[CO32-] b��[HCO3-]��[HC2O4-]��[C2O42-]��[CO32-]
c��[H+]��[HC2O4-]��[C2O42-]��[CO32-] d��[H2CO3] ��[HCO3-]��[HC2O4-]��[CO32-]
��4������ѪҺ�е�̼���̼�����δ���ƽ�⣺H++ HCO3- H2CO3�������������Ի�������ʽ���ѪҺ��ʱ��ѪҺ��pH�仯������ƽ���ƶ�ԭ��������������
H2CO3�������������Ի�������ʽ���ѪҺ��ʱ��ѪҺ��pH�仯������ƽ���ƶ�ԭ��������������
________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���㽭����Чʵ��ѧ��һ�����л�ѧ����ѡ�����������棩 ���ͣ�ѡ����
��������£���Ӧ������ͬ���� ( )
A�������0.1 mol/L HCl��0.1 mol/L H2SO4�ֱ���0.2 mol/L NaOH��Һ��Ӧ
B��������п����п�۷ֱ������1 mol/L HCl��Ӧ
C���������Ũ��HCl��HNO3�ֱ����������Na2CO3��ĩ��Ӧ
D�������0.2 mol/L HCl��0.1 mol/L H2SO4������ȱ������״ʯ��ʯ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���㽭����Чʵ��ѧ��һ�����л�ѧ���������������棩 ���ͣ������
ij�¶��£�ˮ�����ӳ���KW��10��13�������¶���pH��11��Ba(OH)2��ҺaL��pH��1��H2SO4��ҺbL��ϣ�������Һ���Ϊ����֮�ͣ����ù���������Բ��ơ�
��1�������û����ҺΪ���ԣ���a:b��________�����ɳ������ʵ���Ϊ______mol(�ú�b����ʽ����ʾ)��
��2����a:b��9:2����������ҺpH��_____���û����Һ������ܽ�����_______g(�ú�a��b����ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���㽭����Чʵ��ѧ��һ�����л�ѧ���������������棩 ���ͣ�ѡ����
���淴Ӧ��X(g)+2Y(g) 2Z(g)��2M(g)
2Z(g)��2M(g) N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ(�������෴Ӧ���¶���ͬ)�������ж���ȷ���ǣ�
N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ(�������෴Ӧ���¶���ͬ)�������ж���ȷ���ǣ�

A����Ӧ�ٵ�����Ӧ�����ȷ�Ӧ
B����ƽ��( I)ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
I)ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C����ƽ��(I)ʱX��ת����Ϊ5/11
D����ƽ��(I)��ƽ��(II)��M�����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���㽭����Чʵ��ѧ��һ�����л�ѧ���������������棩 ���ͣ�ѡ����
�������ֶ�����Ԫ�ص�ijЩ���������ʾ(����ֻ��W��Y��ZΪͬ����Ԫ��)��
Ԫ�ش��� | X | W | Y | Z | Q |
ԭ�Ӱ뾶(��10��12 m) | 37 | 64 | 66 | 70 | 154 |
��Ҫ���ϼ� | ��1 | ��1 | ��2 | ��5����3 | ��1 |
����˵����ȷ����( )
A����Q��Y�γɵĻ�������ֻ�������Ӽ�
B��Z��X֮���γɵĻ�������л�ԭ��
C����X��Y��Z����Ԫ���γɵĻ�����侧��һ���Ƿ��Ӿ���
D��Y��W�γɵĻ����Y�Ը���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���㽭����Чʵ��ѧ��һ�����л�ѧ���������������棩 ���ͣ�ѡ����
��һ�̶�������ܱ������м���2 mol A��1 mol B������Ӧ2A(g)+B(g) 4C(g)+D(s)���ﵽƽ��ʱC��Ũ��Ϊw mol��L-1����ά��������������¶Ȳ��䣬������������ȷ�����Ϊ��Ӧ���ƽ���ʹC��Ũ����Ϊw mol��L-1�������()
4C(g)+D(s)���ﵽƽ��ʱC��Ũ��Ϊw mol��L-1����ά��������������¶Ȳ��䣬������������ȷ�����Ϊ��Ӧ���ƽ���ʹC��Ũ����Ϊw mol��L-1�������()
A.4 molA+2 molB
B.4 mol C+1 molD+2mol A+1 mol B
C. 1.6mol C+0.3 molD+1.2mol A+0.6 mol B
D. 4 mol C+0.8molD
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭���ݶ��и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ѧѧ���ڸ�����ҵ���������������һ�����ڱ�д���֡���Ȥζʵ�顣��ֽ�����Ȼ��ơ���ɫ��̪�Ļ��Һ��ʪ��Ȼ��ƽ����һ�鲬Ƭ�ϣ���ͨ��Դ����Ǧ������ֽ��д�֣�����ֺ�ɫ�ּ����ݴˣ�����������ȷ����( )
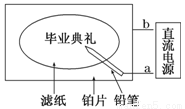
A��Ǧ�ʶ�������������������Ӧ
B����Ƭ��������������������Ӧ
C��Ǧ�ʶ�����������������
D��a���Ǹ�����b��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ��һ��ͨ�������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
25�桢101kPaʱ��1g�״���ȫȼ������CO2��Һ̬H2O��ͬʱ�ų�22.68kJ���������б�ʾ�÷�Ӧ���ȷ���ʽ��ȷ����
A��CH4O(l)+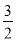 O2(g)=CO2(g)+2H2O(g)����H=��725.8kJ�� mol��1
O2(g)=CO2(g)+2H2O(g)����H=��725.8kJ�� mol��1
B��2CH4O(l)+3O2(g)=2CO2(g)+4H2O(l)����H=+1451.6kJ�� mol��1
C��2CH4O(l)+3O2(g)=2CO2(g)+4H2O(l)����H=��22.68kJ�� mol��1
D��CH4O(l)+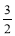 O2(g)=CO2(g)+2H2O(l)����H=��725.8kJ�� mol��1
O2(g)=CO2(g)+2H2O(l)����H=��725.8kJ�� mol��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com