
【题目】NA代表阿伏加德罗常数的值。下列叙述错误的是
①18g金刚石中,碳碳共价键数为3NA
②1mol铜与足量硫蒸气反应,转移的电子数为NA
③常温常压下,S2和S6的混合物共6.4g,其中所含硫原子数一定为0.2NA
④一定温度下,1L 0.50mol L-1NH4Cl溶液与2L 0.25molL-1NH4Cl溶液中的NH4+的数目均少于0.5NA,且前者更少
⑤电解法精炼铜时,当阳极质量减少64g时,电路中通过的电子数一定为2NA
A. ②B. ②④⑤C. ④⑤D. ②④
【答案】C
【解析】
①n(C)=![]() =1.5mol,金刚石属于原子晶体,其中n(C):n(C-C)=1:2,则含有的碳碳共价键为3mol,个数为3NA,故正确;
=1.5mol,金刚石属于原子晶体,其中n(C):n(C-C)=1:2,则含有的碳碳共价键为3mol,个数为3NA,故正确;
②Cu与S反应生成Cu2S,Cu元素的化合价由0价升至+1价,1molCu完全反应转移1mo电子,个数为NA,故正确;
③S2和S8的混合物中只有S元素,n(S)=![]() =0.2mol,个数为0.2NA,故正确;
=0.2mol,个数为0.2NA,故正确;
④由于NH4+的水解,两溶液中NH4+物质的量都小于0.5mol,NH4Cl的浓度越小,NH4+的水解程度越大,后者NH4+更少,故错误;
⑤电解精炼铜,阳极为粗铜,阳极电极反应有:Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,粗铜中活泼性不如Cu的杂质以阳极泥的形式沉降,由于阳极中各杂质的比例未知,无法计算电路中通过电子的物质的量,故错误;
故选C。


科目:高中化学 来源: 题型:
【题目】在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g)![]() cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是

A. 在图象反应Ⅰ中,说明正反应为吸热反应
B. 在图象反应Ⅰ中,若p1>p2,则此反应的ΔS>0
C. 在图象反应Ⅱ中,说明该正反应为吸热反应
D. 在图象反应Ⅲ中,若T1>T2,则该反应能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质是人类生活的基本营养物质,下列叙述不正确的是
A.葡萄糖是单糖B.淀粉是糖类物质,它遇碘化钾迅速变蓝
C.蛋白质烧焦时可产生特殊气味D.油脂在碱性条件下水解可以制肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向10mL0.1mol/L的HR溶液中逐滴加入0.1mol/L的氨水,所得溶液pH及导电性变化如图。下列分析正确的是

A. a~c点,溶液中离子数目先增大后减小
B. b点溶液pH=7说明c(NH4+)=c(R-)
C. c点溶液存在c(NH4+)>c(R-)>c(H+)>c(OH-)
D. b、c两点对应溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是药物合成中的一种重要中间体,下面是G的一种合成路线:
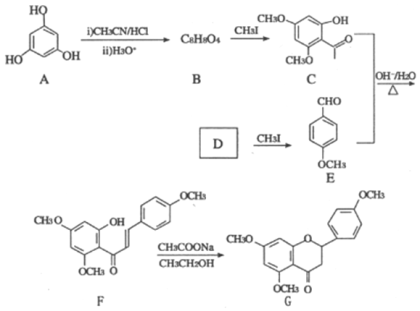
回答下列问题:
(1)B的结构简式为__________,其中所含官能团的名称为__________;B生成C的反应类型为__________。
(2)D的名称是__________。
(3)由C和E合成F的化学方程式为________________________________________。
(4)D的同分异构体中,能发生银镜反应且分子结构中含苯环的还有__________种,其中核磁共振氢谱上有6组峰,峰面积之比为1∶1∶1∶1∶1∶1的同分异构体的结构简式为______________________ (一种即可)。
(5)参照上述合成路线,以CH3CH2Cl为原料(其他试剂任选),设计制备巴豆醛(CH3CH=CH
CHO)的合成路线。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
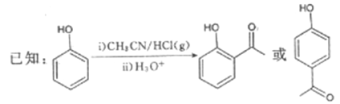
我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________。
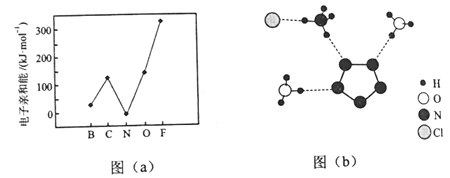
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5-中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则N5-中的大π键应表示为____________。
),则N5-中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____________、____________。
(4)R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在平衡I2(aq)+I(aq)=I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上的任何点都表示平衡状态)。下列说法正确的是

①I2(aq)+I—(aq)=I3—(ag) ΔH>0
②若温度为T1、T2时反应的平衡常数分别为K1、K2,则K1>K2
③若反应进行到状态D时,一定有v正>v逆
④状态A与状态B相比,状态A的c(I2)大
⑤保持温度不变,向该混合溶液中加水,![]() 将变大
将变大
A. 只有①②B. 只有②③C. ①③④D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g)ΔH=-226kJ/mol
O2(g)ΔH=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为283 kJ
B. 如图可表示由CO生成CO2的反应过程和能量关系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com