
| A. | 150mL 1mol/L 的NaCl溶液 | B. | 75mL 2mol/L的NH4Cl溶液 | ||
| C. | 100mL 1.5mol/L的KCl溶液 | D. | 75mL 1.5mol/L的CaCl2溶液 |
分析 氯离子的物质的量浓度与溶液体积大小无关,与溶质组成及溶质的浓度有关,如:50mL 1mol/L AlCl3溶液中c(Cl-)=1mol/L×3=3mol/L,据此进行解答.
解答 解:50mL 1mol/L AlCl3溶液中c(Cl-)=1mol/L×3=3mol/L,
A.150mL 1mol/L 的NaCl溶液中氯离子浓度为1mol/L,故A错误;
B.75mL 2mol/L的NH4Cl溶液中氯离子的浓度为2mol/L,故B错误;
C.100mL 1.5mol/L的KCl溶液中氯离子浓度为1.5mol/L,故C错误;
D.75mL 1.5mol/L的CaCl2溶液中氯离子的浓度为:1.5mol/L×2=3mol/L,故D正确;
故选D.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意离子浓度与溶液体积大小无关,为易错点,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
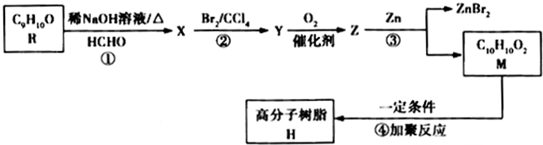
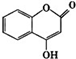 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成: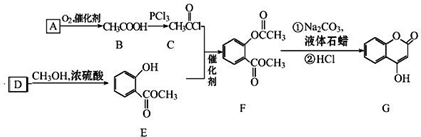
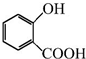 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$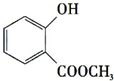 +H2O;
+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
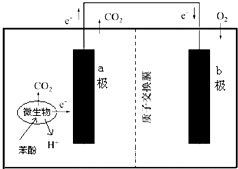
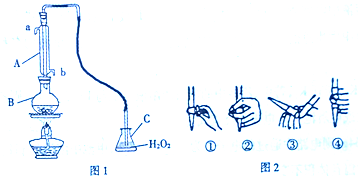
| A. | 该装置可将化学能转化为电能 | |
| B. | 溶液中H+由a极移向b极 | |
| C. | 电极b附近的pH降低 | |
| D. | 电极a附近发生的反应是:C6H6O-28e-+11H2O$\stackrel{微生物}{→}$6CO2+28H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
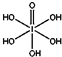 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
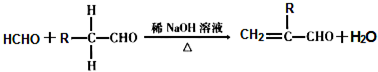
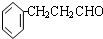 .
.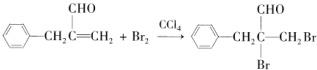 .
.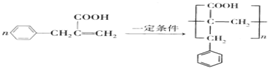 .
.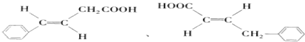 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2A、NaHA两溶液中,离子种类不相同 | |
| B. | 在溶质的物质的量相等的Na2A,NaHA两溶液中,阴离子总数相等 | |
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-) | |
| D. | 在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com