
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 配制一定物质的量浓度的溶液,定容时俯视刻度线,会使所配溶液浓度偏高 | |
| C. | 二氧化硅不与强酸反应,可用石英作为反应容器制取氢氟酸 | |
| D. | 燃着的镁条伸入盛满二氧化碳的集气瓶中,不能继续燃烧 |
分析 A、在原电池中,负极被腐蚀,正极被保护;
B、配制一定物质的量浓度的溶液,定容时俯视刻度线,则溶液体积偏小;
C、二氧化硅和一般的强酸不反应,但能和HF反应;
D、镁能和二氧化碳反应生成MgO和C.
解答 解:A、在原电池中,负极被腐蚀,正极被保护,故将铜块装在轮船上,铜做正极,轮船做负极,腐蚀的速率加快,故A错误;
B、配制一定物质的量浓度的溶液,定容时俯视刻度线,则溶液体积偏小,则溶液的浓度偏高,故B正确;
C、二氧化硅和一般的强酸不反应,但能和HF反应,故不能用石英作为反应容器来制取HF,故C错误;
D、镁能和二氧化碳反应生成MgO和C,故镁能在二氧化碳气体中继续燃烧,故D错误.
故选B.
点评 本题考查了金属的腐蚀防护、配制一定物质的量浓度溶液时的误差分析和二氧化硅的性质等,应注意的是二氧化碳能灭一般的火,但不能灭镁火.


 同步轻松练习系列答案
同步轻松练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 天然气的化学组成主要是烃类气体,以甲烷为主 | |
| B. | 石油中含有1-50个碳原子的烷烃和环烷烃 | |
| C. | 石油的催化重整不可能获得芳香烃 | |
| D. | 石油的催化裂解是工业生产乙烯的重要环节 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它的元素名称为锡 | B. | 它的核外电子排布式为[Ar]4s24p4 | ||
| C. | 它的第一电离能小于As | D. | 其外围电子排布图为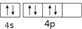 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、甲苯、溴乙烷(酸性高锰酸钾溶液) | B. | 乙醇、乙醛、乙酸(新制Cu(OH)2) | ||
| C. | 苯、乙醇、四氯化碳(溴水) | D. | 苯、己烷、苯酚溶液(浓溴水) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径:Br>Se | |
| B. | 还原性:H2Se>HBr | |
| C. | Se在元素周期表中位于第四周期第六族 | |
| D. | 在Se2Br2分子中只含有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
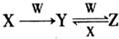 已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.
已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.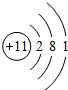 ,用电子式写出C和E形成化合物的过程
,用电子式写出C和E形成化合物的过程 ,用电子式写出A和B形成化合物的过程
,用电子式写出A和B形成化合物的过程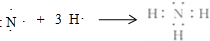 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| n(A)/mol | 0.40 | - | 0.20 | - | - | 0.10 |
| n(B)/mol | 0.00 | 0.24 | - | 0.52 | 0.60 | 0.60 |
| A. | 0~40 s的平均反应速率v(B)=0.01 mol•L-1•s-1 | |
| B. | 80 s时容器中混合气体的密度小于40 s时混合气体的密度 | |
| C. | 其他条件不变,加入合适的催化剂,0~80 s时间段内v(A)>0.001 875 mol•L-1•s-1 | |
| D. | 反应达到最大限度后,增加A的浓度,B的生成速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应2CO(g)→2C(s)+O2(g);△H>0不能自发进行,加入适当的催化剂可以自发 | |
| B. | 粗铜电解精炼时,阳极减少的质量与阴极增加的质量一定相同 | |
| C. | 体积均为10mL pH均为2的盐酸与醋酸,分别加入0.1g Zn,最终醋酸产生的H2多 | |
| D. | 一定条件下反应2NO2(g)?N2O4(g)达到平衡时,v(NO2)逆=2v(N2O4)正 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com