
| A. | H2和D2互为同位素 | |
| B. | 12C原子是指质子数为6,中子数是12的一种核素 | |
| C. | 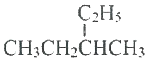 的名称是2-乙基丁烷 的名称是2-乙基丁烷 | |
| D. | 分子式为C2H6O、C4H10的有机物均有两种同分异构体 |
分析 A.质子数相同、中子数不同的原子互为同位素;
B.12C中质量数为12,质量数=质子数+中子数;
C.2号碳上不能有乙基;
D.醇和醚是同分异构体,根据烷烃的碳链异构判断.
解答 解:A.质子数相同、中子数不同的原子互为同位素,H2和D2是分子,不是原子,不是同位素,故A错误;
B.12C中质量数为12,质量数=质子数+中子数,则中子数=12-6=6,故B错误;
C.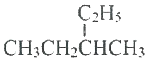 的主链上有5个碳,其名称是3-甲基戊烷,故C错误;
的主链上有5个碳,其名称是3-甲基戊烷,故C错误;
D.分子式为C2H6O的同分异构体有CH3CH2OH、CH3OCH3,C4H10的同分异构体为CH3CH2CH2CH3、CH3CH(CH3)2,故D正确.
故选D.
点评 本题考查同位素的概念、中子数的计算、有机物的命名、同分异构体,题目难度不大,明确质量数、质子数和中子数的关系、以及同位素、同分异构体的概念是解本题关键,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:解答题
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
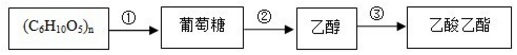
| A. | 反应②的反应类型属于分解反应 | |
| B. | (C6H10O5)n可以是淀粉或纤维素,二者互为同分异构体 | |
| C. | 将烧黑的铜丝趁热插入乙醇中可得到乙酸 | |
| D. | 向反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
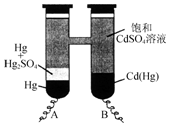 依据Cd(Hg)+Hg2SO4═3Hg+Cd2++SO42-反应原理,设计出韦斯顿标准电池,其简易装置如图.下列有关该电池的说法正确的是( )
依据Cd(Hg)+Hg2SO4═3Hg+Cd2++SO42-反应原理,设计出韦斯顿标准电池,其简易装置如图.下列有关该电池的说法正确的是( )| A. | 电池工作时Cd2+向电极B移动 | |
| B. | 电极A上发生的反应:Hg2SO4+2e-═2Hg+SO42- | |
| C. | 电极B上发生的反应:Cd(Hg)-4e-═Hg2++Cd2+ | |
| D. | 反应中每生成a mol Hg转移3a mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
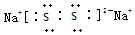 ;所含化学键类型离子键、共价键.
;所含化学键类型离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
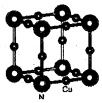 配合物[Cu(CH3C≡N)4]BF4是双烯合成反应的催化剂,它被浓硝酸分解的化学方程式为:[Cu(CH3C≡N)4]BF4$\stackrel{HNO_{3}}{→}$Cu2++H3BO3+CO2↑+HF…(未配平).
配合物[Cu(CH3C≡N)4]BF4是双烯合成反应的催化剂,它被浓硝酸分解的化学方程式为:[Cu(CH3C≡N)4]BF4$\stackrel{HNO_{3}}{→}$Cu2++H3BO3+CO2↑+HF…(未配平).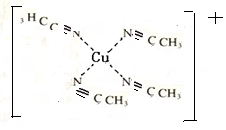 (不考虑空间构型).
(不考虑空间构型).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D与E可形成既含极性键又含非极性键的分子 | |
| B. | B的最高价氧化物为酸性氧化物,不能与任何酸反应 | |
| C. | B、C、E三种元素的最高价氧化物对应的水化物中,B的酸性最弱 | |
| D. | A、C、D中两种或三种元素形成的钠盐溶液可显酸性、中性或碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
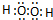 .
. ,用电子式表示A2C的形成过程.
,用电子式表示A2C的形成过程.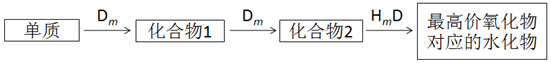
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
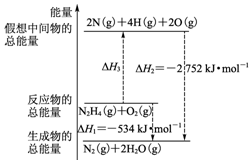 断裂1mol化学键所需的能量如表:
断裂1mol化学键所需的能量如表:| 化学键 | N-N | O=O | N≡N | N-H |
| 键能(kJ) | 154 | 500 | 942 | a |
| A. | N2比O2稳定 | |
| B. | N2H4(g)+O2(g)?N2(g)+2H2O(g)△H=-534 kJ•mol-1 | |
| C. | 表中的a=194 | |
| D. | 图中的△H3=+2218 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com