
【题目】化学与科学、技术、社会、环境密切相关,下列有关说法中错误的是
A. 春节燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰
C. 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
D. 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢
科目:高中化学 来源: 题型:
【题目】为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是

A. N极是负极
B. 该装置工作时,H+从右侧经阳离子交换膜移向左侧
C. 负极的电极反应为:(C6H10O5)n+7H2O﹣24e﹣═6CO2↑+24H+
D. 物质X是OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某待测溶液(阳离子为Na+)中可能含有SO42-、SO32-、Cl-、Br-、CO32-、HCO3-中的一种或多种,进行如下图所示的实验,每次实验所加试剂均过量。已知稀HNO3具有强氧化性。下列说法不正确的是( )

A. SO42-、SO32-至少含有一种 B. 沉淀B的化学式为 BaCO3
C. 肯定存在的阴离子有 CO32-、HCO3-、Cl- D. Br—肯定不存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H是一种合成药物的中间体,H的合成方案如下:

已知: ![]()
请回答下列问题:
(1)A为相对分子质量为104的芳香烃,A的实验式为___________
(2)可鉴别A和C两种有机物的试剂为(答出一种即可)___________________________
(3)F为一氯代物,其核磁共振氢谱有三个吸收峰,则E的结构简式为________________
(4)写出B→C的化学方程式____________________________________________________
(5)写出D和G生成H的化学方程式_____________________________________________
(6)D的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应的有__________种,写出其中核磁共振氢谱中吸收峰数目最少的结构简式__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:HCO3-+H+= CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-![]() Cl2↑+Mn2++H2O
Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu = Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液中,探究Fe2+和I-的还原性强弱。
[提出假设] 假设1:Fe2+还原性比I-强。
假设2:I-还原性比Fe2+强。
[验证假设] 选择几种装置进行实验:

(1)实验必需的装置是A→____________(按Cl2气流方向的顺序填写)。
(2)实验开始后,控制通入氯气的量,当通入少量氯气时,通过观察混合溶液颜色的变化________(填“能”或“不能”)判断反应的先后顺序。
(3)请在下表中写出实验步骤及预期现象和结论________、________、________、________、_______、________。

(4)为了实验成功,必须控制各物质的量。该小组称取1.52g FeSO4固体,同时称取1.66g KI固体,溶于水中配成混合溶液。为了验证上述假设,通入的Cl2体积最多不能超过________L(标准状况)。
[思考与交流]
(5)有同学质疑,上述实验中Cl2量很难控制,无法验证Fe2+和I-反应的先后顺序。于是提出另一方案:往KI溶液中滴入________溶液,如果能发生反应,即可证明I-的还原性强于Fe2+。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】有机物E是医药合成中间体.其合成路线如图:
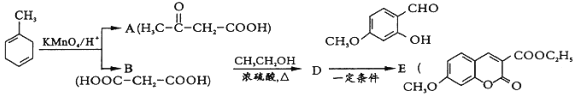
(1)![]() 的官能团名称为______.
的官能团名称为______.
(2)已知![]() 的系统命名为 2-丙酮酸,则A的名称是________________.
的系统命名为 2-丙酮酸,则A的名称是________________.
(3)D为二元酯,则B→D的化学方程式为________________________________________.
D→E的反应历程如图:

(4)写出这几步的反应类型:I_____________,Ⅱ____________III____________
(5)![]() 中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
(6)写出满足下列条件的D的所有同分异构体的结构简式______________________________.
a.核磁共振氢谱有3组峰
b.常温下能与NaHCO3按1:2反应并释放出气体
(7)由化合物A经过两步便可以合成环境友好型高聚物聚3-羟基丁酸酯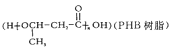
请写出反应合成线路,结合已知信息选用必要的无机试剂,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com