

分析 ①由图可知,X越大,转化率越低;
②分解反应为吸热反应,温度高,转化率大.
解答 解:①由图可知,X越大,转化率越低,升高温度转化率增大,则X表示压强,故答案为:压强;
②由SO3(g)=SO2(g)+O2(g)△H>0,温度高,转化率大,图中等压强时L2对应的转化率大,则L1<L2,
故答案为:<;SO3(g)分解的热化学方程式为2SO3(g)=2SO2(g)+O2(g)△H=+196kJ•mol-1,当压强一定时,温度升高,平衡转化率增大.
点评 本题考查化学平衡影响因素分析,为高频考点,把握发生的反应、平衡影响因素为解答的关键,侧重分析与应用能力的综合考查,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入硝酸银溶液时有白色沉淀,说明溶液中含有Cl- | |
| B. | 加入BaCl2产生白色沉淀,加入稀盐酸不溶解,说明溶液中含有SO42- | |
| C. | 加入NaOH溶液,加热产生无色刺激性能使湿润的红色石蕊试纸变蓝的气体,说明溶液中一定含有NH4+ | |
| D. | 加入氢氧化钡溶液时,有白色沉淀生成,再加稀盐酸时,白色沉淀溶解,产生可使澄清石灰水变浑浊的无色无味气体,则溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
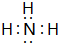 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学的特征是认识分子 | |
| B. | 新制氯水应保存在棕色试剂瓶中,放于阴凉处 | |
| C. | 在化学反应中,参加反应的各物质的质量比等于其物质的量之比 | |
| D. | 英国化学家玻义耳提出原子学说,为近代化学的发展奠定了坚实的基础 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )
在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )| A. | 对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和体积不变,再加入一定量的HI | |
| B. | 对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和压强不变,再加入一定量的HI | |
| C. | 对于PCl5(g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和体积不变,再加入一定量的PCl5 | |
| D. | 对于PCl5 (g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和压强不变,再加入一定量的PCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验Cl-离子的试剂是硝酸银和硝酸 | |
| B. | 配制一定物质的量浓度溶液时,未洗涤烧杯和玻璃棒,结果会偏低 | |
| C. | 配制一定物质的量浓度溶液时,容量瓶中有少量蒸馏水,对浓度无影响 | |
| D. | 向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| C-F | 427 | C-Cl | 330 | C-I | 218 |
| H-H | 436 | S=S | 255 | H-S | 339 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol${\;}_{8}^{16}$OD-含有的质子、中子数均为9NA | |
| B. | 3.6g石墨和C60的混合物中,含有的碳原子数为0.3NA | |
| C. | 含有4.6g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| D. | 标准状况下,4.48L HF含有的分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com