
【题目】下列是实验室制取Cl2并以Cl2为原料进行特定反应的实验:

(1)A为氯气发生装置,写出反应的化学方程式_____________________.
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯.Cl2通入C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(气),试写出D装置中反应的化学方程式_______________.装置C的作用是________________.
(3)E处石蕊试液的现象是_____________,其原因是________________.
(4)若将E处溶液改为澄清石灰水,反应过程的现象是___________.
A.有白色沉淀生成 B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________________________________________.B的作用是___________________________________________.
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 2Cl2+C+2H2O
MnCl2+Cl2↑+2H2O 2Cl2+C+2H2O![]() CO2+4HCl 提供反应需要的H2O 先变红,后褪色 D中生成HCl使溶液变红,而剩余的Cl2生成的HClO使红色溶液褪色 B B中液面下降,长颈漏斗内液面升高 充当储气瓶、安全装置、使内压降低
CO2+4HCl 提供反应需要的H2O 先变红,后褪色 D中生成HCl使溶液变红,而剩余的Cl2生成的HClO使红色溶液褪色 B B中液面下降,长颈漏斗内液面升高 充当储气瓶、安全装置、使内压降低
【解析】
由装置中的信息可知,A装置是用于制备氯气的,B装置是用于除去氯气的氯化氢并且也是储气装置,C装置为D装置提供水蒸气,E装置是尾气处理装置,并可检验氯气与水反应的产物的性质。
(1)A为氯气发生装置,是氯气的实验室制法,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 。
MnCl2+Cl2↑+2H2O 。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯.Cl2通入C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(气), D装置中反应的化学方程式为2Cl2+C+2H2O![]() CO2+4HCl,装置C的作用是提供反应需要的H2O。
CO2+4HCl,装置C的作用是提供反应需要的H2O。
(3)E处石蕊试液的现象是先变红,后褪色,其原因是:D中生成HCl使溶液变红,而剩余的Cl2生成的HClO使红色溶液褪色。
(4)若将E处溶液改为澄清石灰水,氯气可以与其反应生成可溶性的氯化钙和次氯酸钙,溶液中不会有沉淀生成,故反应过程的现象是:无白色沉淀生成。选B。
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,将把B中的饱和食盐水排入长颈漏斗中,此时B中的现象是:B中液面下降,长颈漏斗内液面升高。B的作用是:充当储气瓶,安全装置,使内压降低。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
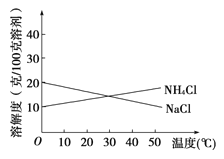
【题目】联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如图所示,以下操作正确的是( )
通入气体 | 温度控制 | |
A | CO2 | 30~40℃ |
B | CO2 | 0~10℃ |
C | NH3 | 30~40℃ |
D | NH3 | 0~10℃ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用0.1000 mol·L1的NaOH标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
A.___________________________。
B.分别用蒸馏水洗干净酸式滴定管和碱式滴定管。
C.用待测定的盐酸溶液润洗酸式滴定管。
D.用酸式滴定管取稀盐酸 25.00 mL,注入事先洗干净的锥形瓶中,加入指示剂。
E.碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至刻度“0”或“0”刻度以下。
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
G.另取锥形瓶,再重复操作一次。
(1)定滴管在使用前需进行的操作A是___________________________。
(2)滴定实验所需的玻璃仪器有______________。(填字母)
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶
E.铁架台 F.滴定管夹 G.烧杯 H.白纸
(3)该小组同学选用酚酞做指示剂,滴定终点的现象为________________________________。
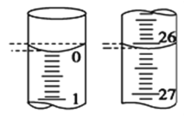
(4)该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,
则本次滴入的盐酸体积为 ___________ mL。
(5)该小组学生某3次实验的有关数据分别记录如下表:
滴定次数 | 待测HCl溶液的体积/mL | 0.1000 mol/LNaOH的体积(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 2.00 | 27.91 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
依据上表数据列式计算该HCl溶液的物质的量浓度为_______________。
(6)下列操作中可能使测定结果偏低的是___________(填字母)。
A.酸式滴定管未润洗就直接注入待测液HCl溶液
B.滴定前盛放HCl溶液的锥形瓶用蒸馏水洗净后没有干燥
C.碱式滴定管尖嘴部分在滴定前有气泡,滴定后气泡消失
D.读取NaOH标准液时,开始仰视读数,滴定结束时俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g)= 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
(2)C(s)+O2(g)= CO2(g) ΔH2=-393.5 kJ/mol
(3)H2(g)+![]() O2(g)= H2O(l) ΔH3=-285.8 kJ/mol
O2(g)= H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)= CH3COOH(l)的焓变为( ).
A.-488.3 kJ/molB.-244.15 kJ/molC.488.3 kJ/molD.244.15 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入X和Y,在一定条件下进行如下反应:aX(g)+bY(g) ![]() cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是
cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是

A.由图I得K(200℃)>K(400℃),但a+b与c+d的大小无法比较
B.若a=c,在保持Y浓度不变的前提下,使X和Z的浓度增大相同的倍数,平衡正向移动
C.若反应在恒容容器中进行,达平衡后再充入气体Z,由于压强增大,平衡正向移动
D.该反应在不同温度下(T2>T1),Z的体积分数与时间的关系图象可用图Ⅱ表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe![]() Sb4O6+6FeS,
Sb4O6+6FeS,
②Sb4O6+6C![]() 4Sb+6CO↑。关于反应①、②的说法正确的是
4Sb+6CO↑。关于反应①、②的说法正确的是
A.反应①、②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3molFeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是

A.S2Cl2的结构式为Cl—S—S—Cl
B.S2Cl2为含有极性键和非极性键的极性分子
C.S2Br2与S2Cl2结构相似,熔沸点S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设某元素原子核内的质子数为m,中子数为n,则下列论述正确的是( )
A.不能由此确定该元素的原子量
B.这种元素的原子量为(m+n)
C.若碳原子的质量为w g,此原子的质量为(m+n)w g
D.核内中子的总质量小于质子的总质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,RSO4(s)+CO32-(aq)RCO3(s)+SO42-(aq)的平衡常数K=1.75×104,Ksp(RCO3)=2.80×10-9,下列叙述中正确的是
A.25℃ 时,RSO4的Ksp约为4.9×10-5
B.将浓度均为6×10-5mol/L的RCl2、Na2CO3溶液等体积混合后可得到RCO3沉淀
C.向c(CO32-)=c(SO42-)的混合液中滴加RCl2溶液,首先析出RSO4沉淀
D.相同温度下,RCO3在水中的Ksp大于在Na2CO3溶液中的Ksp
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com