
 部分难溶物的颜色和常温下的Ksp如下表所示:
部分难溶物的颜色和常温下的Ksp如下表所示:| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | - |
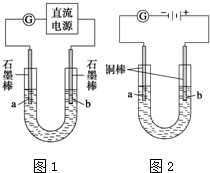
分析 (1)电解饱和食盐水得到的产物是氢氧化钠、氯气和氢气;
(2)在电解氯化钠的装置中,和电源正极相连的是阳极,该极上会产生氯气,和负极相连的是阴极,该极上产生的是氢氧化钠和氢气,根据产物的性质来判断电极;
(3)在电解池的阴极上是阳离子发生得电子的还原反应;
(4)根据题意:电解5min后会产生白色沉淀来回答;
(5)根据表中物质的颜色,CuOH是黄色,但是其不稳定易分解为砖红色的氧化亚铜来回答判断.
解答 解:(1)电解饱和食盐水得到的产物是氢氧化钠、氯气和氢气,故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
(2)电解氯化钠的装置中,和电源正极相连的是阳极,该极上会产生氯气,和负极相连的是阴极,该极上产生的是氢氧化钠和氢气,
A.电解池的阳极上可以产生氯气等有颜色的气体,还可以产生氧气等无色气体,故观察两极产生气体的颜色不可以判断正负极,故A错误;
B.往U形管两端分别滴入数滴酚酞试液,变红色的即是阴极,对应的是电源的负极,故B正确;
C.用燃着的木条靠近U形管口,只能检验有氢气或是氧气产生时的电极反应,但是对其他物质的产生无法检验,故C错误;
D.在U形管口置一张湿润的淀粉KI试纸,能使湿润的淀粉KI试纸变蓝证明氯气的产生,该电极是阳极,对应的是电源的正极,故D正确.
故答案为:BD;
(3)a极是阴极,在电解池的阴极上是水中的阳离子氢离子发生得电子的还原反应:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑),
故答案为:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑);
(4)根据题意知道电解5min后,b极产生的白色沉淀,从表中知道,该物质是CuCl,所以该极上发生的电极反应方程式为Cu+Cl--e-═CuCl↓,
故答案为:Cu+Cl--e-═CuCl↓;
(5)根据题意结合表中物质的颜色知道:12min后,b极附近出现的橙黄色沉淀的成分是CuOH和Cu2O,因为Ksp(CuOH)<Ksp(CuCl),所以电解过程中CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,导致物质的颜色为橙色,
故答案为:CuOH和Cu2O;Ksp(CuOH)<Ksp(CuCl),CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,所以橙黄色沉淀的成分为CuOH和Cu2O的混合物.
点评 本题是一道有关电解池的工作原理的综合考查题,要求学生具有分析和解决问题的能力,难度较大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 向Ge(OH)4中加入盐酸:OH-+H+═H2O | |
| B. | MnO2 与浓盐酸反应制Cl2:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O | |
| C. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| D. | 双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 氯化钙溶液与碳酸钠溶液反应:Ca2++CO32-═CaCO3↓ | |
| C. | 硫酸溶液与碳酸钡反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑦ | B. | ②⑥⑦ | C. | ②④⑤⑥⑦ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
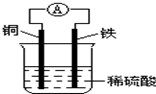
| A. | 铜棒逐渐溶解 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 负极反应式为Fe-2e-=Fe2+,发生还原反应 | |
| D. | 电子由铁棒通过导线流向铜棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
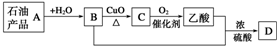
| A. | A能使酸性高锰酸钾溶液褪色 | B. | 可用B萃取碘水中的碘单质 | ||
| C. | B与乙酸发生了取代反应 | D. | D的结构简式为CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
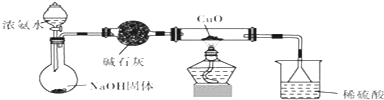
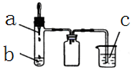 利用如图所示装置进行下列实验,实验现象与结论均正确的是( )
利用如图所示装置进行下列实验,实验现象与结论均正确的是( )| 选项 | 实验试剂 | 实验现象 | 实验结论 | ||
| a | b | c | |||
| A | 浓氨水 | 碱石灰 | FeCl2溶液 | 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 | 氨气具有氧化性 |
| B | 稀硫酸 | FeS | AgCl悬浊液 | 悬浊液由白色变为黑色 | Ksp(AgCl)>Ksp(Ag2S) |
| C | 浓硝酸 | 铜 | BaSO3悬浊液 | 悬浊液变澄清 | +4价硫具有还原性 |
| D | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com