
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素原子的内层电子数是最外层电子数的一半,则下列说法正确的是( )
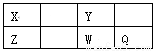
A.W的一种核素质量数是A,则其中子数是A-16
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
科目:高中化学 来源:2015-2016学年广东省汕头市高二下期末化学试卷(解析版) 题型:选择题
下列物质的分离提纯所用的方法不正确的是
A.酒精和水--分液
B.淀粉溶液中混有氯化钠--用半透膜进行渗析
C.汽油和柴油--分馏
D.三氯甲烷和水--分液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中理综化学试卷(解析版) 题型:填空题
硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:①SiO2 + 2C Si + 2CO
Si + 2CO
精炼硅:②Si + 3HCl SiHCl3 + H2
SiHCl3 + H2
③SiHCl3 + H2 Si + 3HCl
Si + 3HCl
化学反应与能量变化如图所示,回答下列问题:
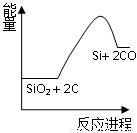
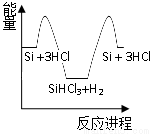
(1)反应①是_________反应(填“吸热”或“放热”),反应②是_________反应(填“吸热”或“放热”)。
(2)反应③破坏反应物中的化学键所吸收的能量_________形成生成物中化学键所放出的能量(填“大于”或“小于”)。
(3)研究物质变化时,人们可以从不同角度、不同层面来认识物质变化时所引起的化学键及能量变化。据此判断下列说法错误的是_________(双选)。
A.金属钠和氯气反应生成 氯化钠后,其结构的稳定性增强,体系的能量降低
氯化钠后,其结构的稳定性增强,体系的能量降低
B.等量的硫蒸气 和硫固体分别完全燃烧,前者放出的能量多
和硫固体分别完全燃烧,前者放出的能量多
C.氮气分子内部存在着很强的共价键,故通常状况下氮气的化学性质很活泼
D.由石墨制取金刚石是吸热反应,可知金刚石比石墨稳定
E.由放热反应H2 + Cl2 ====  2HCl来说,断裂1mol H—H键和1molCl—Cl键所吸收的能量小于形成2molH—Cl键所放出的能量
2HCl来说,断裂1mol H—H键和1molCl—Cl键所吸收的能量小于形成2molH—Cl键所放出的能量
(4)在研究化学反应中的能量变化时,我们通常做下面 的实验:
的实验:
在一个小烧杯里,加入20g已经研磨成粉末的氢氧化钡晶体【Ba(OH)2.8H2O】,将小烧杯放 在事先已滴有3—4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒迅速搅拌。写出实验过程中发生反应的化学方程式_________,该反应中反应物总能量_________生成物的总能量(填“大于”或“小于”),实验过程中立即用玻璃棒迅速搅拌的原因是_________。
在事先已滴有3—4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒迅速搅拌。写出实验过程中发生反应的化学方程式_________,该反应中反应物总能量_________生成物的总能量(填“大于”或“小于”),实验过程中立即用玻璃棒迅速搅拌的原因是_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
100 mL KNO3和Cu(NO3)2的混合溶液中c(NO3—)=6.0 mol/L,用石墨作电极电解此溶液,通电一段时间后,两极均收集到4. 48 L气体(标准状况),假定电解后溶液体积仍为100 mL,下列说法不正确的是( )
48 L气体(标准状况),假定电解后溶液体积仍为100 mL,下列说法不正确的是( )
A.原混合溶液中c(K+)=2mol/L
B.上述电解过程中一共转移电子0.8 mol
C.电解得到的铜的物质的量为0.2 mol
D.电解后溶液中c(H+)=2 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其 过程
过程 如下:mCeO2
如下:mCeO2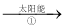 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+ xCO2 mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
下列说法不正确的是( )
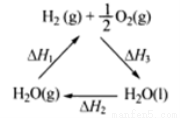
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中△H1=△H2+△H3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol。则 H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是 283.0 kJ/mol,则2CO2(g)===2CO(g) +O2(g)反应的ΔH=+2×283.0 kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期中化学试卷(解析版) 题型:选择题
聚碳酸酯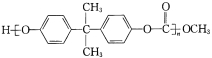 透光率好,可制作车、船、飞机的挡风玻璃。它是由碳酸二甲酯 CH3O-CO-OCH3 与下列哪种物质缩聚而成的( )
透光率好,可制作车、船、飞机的挡风玻璃。它是由碳酸二甲酯 CH3O-CO-OCH3 与下列哪种物质缩聚而成的( )
A.二酚类 B.二卤化物 C.二醛类 D.二烯类
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期中化学试卷(解析版) 题型:选择题
下列关于价电子构型为4s24p4的基态原子描述正确的是( )
A.它的元素名称为锡 B.它的核外电子排布式为[Ar]4s24p4
C.它的第一电离能小于As D.其外围电子排布图为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高一下期中化学试卷(解析版) 题型:填空题
SO2 、NO、NO2 、CO都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。
(1)上述四种气体中直接排入空气时会引起酸雨的有__________(填化学式)。
(2)已知:2SO2 (g)+ O2 (g) 2SO3 (g);△H=-196.6kJ/mol O2 (g)+2NO(g)=2NO2 (g);△H=-113.0kJ/mol
2SO3 (g);△H=-196.6kJ/mol O2 (g)+2NO(g)=2NO2 (g);△H=-113.0kJ/mol
①反应:NO2 (g) +SO2 (g)= SO3 (g) +NO(g)的△H=________ kJ/mol。
②一定条件下,将NO2 和SO2 以体积比1:1置于恒温恒容的密闭容器中发生反应: NO2 (g) +SO2 (g)  SO3 (g) +NO(g),下列不能说明反应达到平衡状态的是___
SO3 (g) +NO(g),下列不能说明反应达到平衡状态的是___ __(填字母)。
__(填字母)。
a.体系压强保持不变
b.混合气体的颜色保持不变
c.NO的物质的量保持不变
d.每生成1molSO3 的同时消耗1molNO2
(3)CO可用于合成甲醇,其反应的化学方程式为CO(g)+2H2 (g)  CH3OH(g)。在一容积可变的密闭容器中充有10molCO和20mol H2 ,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。
CH3OH(g)。在一容积可变的密闭容器中充有10molCO和20mol H2 ,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。
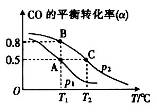
①上述合成甲醇的反应热△H______0(填“<”或“>”)。
②A、B、C三点的平衡常数KA 、KB 、KC的大小关系为___________。
③若达到平衡状态A时,容器的体积为10L,则下列描述正确的是_________。
A.反应体系的压强保持不变
B.体系中氢气浓度保持不变
C.混合气体的的平均摩尔质量保持不变
D.生成甲醇的速率与消耗CO的速率相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com