
在已经处于化学平衡的体系中,如果下列量发生变化,化学平衡一定发生了移动的是
A.反应混合物的浓度 B.反应体系的压强
C.正、逆反应的速率 D.反应体系的温度
科目:高中化学 来源: 题型:
已知101KPa时辛烷的标准燃烧热为—5518kJ·mol-1,含20gNaOH的稀溶液与稀盐酸充分反应放出热量28.7kJ,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(g); △H = +5518 kJ·mol-1
②C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(l); △H = -5518 kJ·mol-1
③H+(aq)+ OH-(aq)= H2O(l); △H = -57.4 kJ·mol-1
④HCl (aq) + NaOH(aq) =NaCl(aq) + H2O(l); △H = —28.7 kJ·mol-1
A.①③ B.②③ C.②④ D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是给病人输液用的氯化钠注射溶液的标签。(友情提示:若要用到溶液密度,可用水的密度进行计算)

(1)氯化钠的摩尔质量____________________
(2)该注射溶液的物质的量浓度为 mol/L。(保留两位有效数字)
(3)某同学配制了1000mL氯化钠注射溶液,为测定所配氯化钠注射液是否达标,取该氯化钠注射液130 mL于烧杯中,然后滴入足量的AgNO3溶液,充分反应后,过滤得到白色沉淀2.87g。请你通过计算判断该氯化钠注射液是否符合上述要求,写出计算过程。
(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。正确的操作顺序是( )
A.③②①⑤④ B.①②③⑤④
C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列混合溶液中,各离子浓度的大小顺序正确的是
A.10 mL0.1 mol·L-1NH4Cl溶液与5 mL0.2 mol·L-1NaOH溶液混合,
c(Na+)=c(Cl-)>c(OH-)>c(H+)
B.10 mL0.1 mol·L-1氨水与10 mL0.1 mol·L-1盐酸混合,
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.10 mL0.1 mol·L-1CH3COOH溶液与10 mL0.2 mol·L-1NaOH溶液混合,
c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10 mL0.5 mol·L-1CH3COONa溶液与5 mL1 mol·L-1盐酸混合,
c(Cl-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表格中的各种情况,可以用下图的曲线表示的是
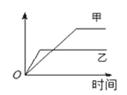
| 反 应 | 纵坐标 | 甲 | 乙 | |
| A | 相同质量的氨,在同一容器中2NH3 | 氨气的转化率 | 500℃ | 400℃ |
| B | 等质量等颗粒大小的钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
| C | 在体积可变的恒压容器中,体积比1︰3的N2、H2, N2 + 3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
| D | 2 molSO2和1 molO2,在相同温度下 2SO2 + O2 | SO3物质的量 | 2个大气压 | 10个大气压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于12 g C-12的说法不正确的是( )
A.碳原子的物质的量为1 mol
B.碳原子的个数为NA mol
C.碳原子的个数为NA
D.该原子常被称为标准碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
确认能发生化学平衡移动的是( )
A.化学反应速率发生了改变
B.有气态物质参加的可逆反应达到平衡后,改变压强
C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D.可逆反应达到平衡后,使用催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com