
A.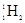 和 和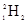 互为同位素,性质相似 互为同位素,性质相似 |
| B.元素的性质随着原子序数的递增呈周期性变化 |
| C.化学反应遵循质量守恒定律相能量守恒定律 |
| D.溶液、浊液、胶体的本质区别是分散质微粒大小不同 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
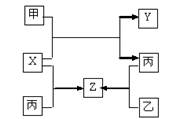
| A.X是具有极性键的非极性分子 | B.Z是水煤气的主要成分之一 |
| C.甲和X的反应是吸热反应 | D.丙是生产硅的重要原料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
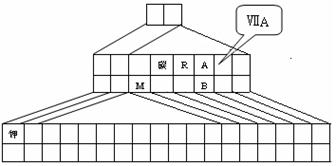
 中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。该离子可能具有的化学性质是_________,依据是_______________________________。
中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。该离子可能具有的化学性质是_________,依据是_______________________________。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 中的①~⑩中元素,用元素符号或化学式填空回答:
中的①~⑩中元素,用元素符号或化学式填空回答: 族 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | | | | ① | | | ② | |
| 三 | ③ | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | ⑩ | | | | | | |
 过程 。
过程 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Z>R>W |
| B.X2W6分子中各原子均满足8电子结构 |
| C.气态氢化物稳定性:HmW>HnR |
| D.Y、Z、R三种元素组成的化合物水溶液一定显碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.12.000 | B.12.009 | C.12.015 | D.12.980 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X:3s23p1 Y:3s23p5 | B.X:2s22p3 Y:2s22p4 |
| C.X:3s23p1 Y:3s23p4 | D.X:3d64s2 Y:2s22p4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 同主族。
同主族。 。
。 式量为392的化合物B,1
式量为392的化合物B,1  mol B中含有6mol结晶水。对化合物B进行如下实验:
mol B中含有6mol结晶水。对化合物B进行如下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com