
分析 二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠的水溶液具有粘性;
根据不同类长石其氧原子的物质的量分数相同,结合化合价代数和是0可写出钙长石的化学式.
解答 解:玻璃中的二氧化硅与NaOH作用生成可用作粘合剂的硅酸钠溶液,反应的方程式为SiO2+2NaOH=Na2SiO3+H2O;由“长石是铝硅酸盐”,结合钠长石的化学式可知钙长石就是将钠长石的中钠更换为钙,铝硅酸阴离子不变,以及化合物中化合价代数和等于0可得钙长石的化学式为CaAl2Si2O8,
故答案为:SiO2+2NaOH=Na2SiO3+H2O;CaAl2Si2O8.
点评 本题考查了化学方程式的书写和化学式的确定,明确二氧化硅的性质是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4能使酸性KMnO4溶液褪色 | |
| B. | 金属Na能与C2H5OH中的甲基反应生成H2 | |
| C. | 乙酸有强烈的刺激性气味,其水溶液称为冰醋酸 | |
| D. | CH3CH2CH2CH3与CH3CH(CH3)2互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 转变为
转变为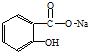 的方法正确的是( )
的方法正确的是( )| A. | 与足量的NaOH溶液共热后,再通入足量的CO2 | |
| B. | 与稀H2SO4共热后,加入足量的Na2CO3 | |
| C. | 与足量的NaOH溶液共热后,加入足量的稀H2SO4 | |
| D. | 与稀H2SO4共热后,加入足量的NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | A | B | C | D |
| △H/(kJ•mol-1) | 10.5 | 1.80 | -126 | -11.7 |
| △S/(J•mol-1•k-1) | 30.0 | -113.0 | 84.0 | -105.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg的化合价由0升高到+2,所以MgO是还原产物 | |
| B. | 由此反应可以判断氧化性CO2>MgO,还原性Mg>C | |
| C. | CO2作氧化剂,表现出氧化性,发生氧化反应 | |
| D. | Mg原子失去的电子数目等于氧原子得到的电子数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3KJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(l);△H=-196.6KJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-78.64KJ•mol-1 | |
| D. | 2SO2(g)+O2(g)?2SO3(g);△H=+196.6KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com