
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) ΔH=-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为____________________。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。
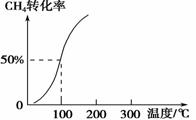 ①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________。
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡c(H2)/c(CH3OH)减小
E.平衡常数K增大
(4) 写出甲醇-空气-KOH溶液的燃料电池负极的电极反应式:______________________。
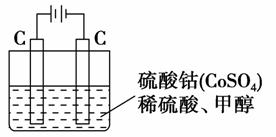 (5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式________。
②写出除去甲醇的离子方程式_______________。
(1)CH4(g)+H2O(g)=CH3OH(g)+H2(g) ΔH=77.0 kJ·mol-1 (2分)
(2)①0.003 mol·L-1·min-1(2分) ②2.25×10-4 (2分)
(3)CD(2分)
(4)CH3OH-6e-+8OH-=CO32-+6H2O(2分)
(5)Co2+-e-=Co3+(2分) 6Co3++CH3OH+H2O=CO2↑+6Co2++6H+(2分)
【解析】(1)写热化学方程式,注意聚集状态,目标反应可由反应Ⅰ、Ⅱ相加得到,计算出反应热。(2)计算速率和平衡常数时要注意容积的体积。计算H2的速率,
方法一:v(H2)=3v(CH4)=3× =0.003 mol·L-1·min-1,
=0.003 mol·L-1·min-1,
方法二:根据“三行式”
CH4(g)+ H2Og= CO(g)+3H2(g)
n(始)/mol 1.0 2.0 0 0
n(变)/mol 0.5 0.5 0.5 1.5
n(平)/mol 0.5 1.5 0.5 1.5
v(H2)= =
= =0.003 mol·-1·min-1
=0.003 mol·-1·min-1
K= =
= =2.25×10-4
=2.25×10-4
(3)体积压缩为原来的一半,则浓度变为原来的2倍,平衡的移动是个“减弱”的过程,浓度比原平衡大,A错误。压强增大,正逆反应速率均增大,B错误。压强增大,平衡向正反应方向移动,C、D正确。平衡常数只与温度有关,E错误。(4)负极上甲醇反应,KOH为电解质,产物为CO32-,“三步书写”。(5)阳极发生氧化反应,Co2+生成Co3+。Co3+将甲醇氧化,生成Co2+和CO2,注意溶液呈酸性。


科目:高中化学 来源: 题型:
用下列实验装置和方法进行相应实验,能达到实验目的的是

A.用图甲装置制取干燥的氨气
B.用图乙装置配制银氨溶液
C.用图丙装置除去CO2中含有的少量HCl
D.用图丁装置吸收NH3,并防止倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组的同学共同设计了如图所示的多功能实验装置。该装置既可用于制取气体,又可用于验证物质的性质。
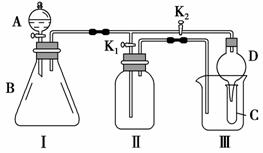
(1)现有以下药品:锌粒、铜片、浓H2SO4、浓HNO3、蒸馏水、NaOH溶液。打开K1,关闭K2,可 制取 ________气体。
制取 ________气体。
(2)某同学用石灰石、醋酸、硅酸钠溶液等药品设计了另一实验。他的实验目的是________________;打开K2,关闭K1,将A中液体加入B中后,观察到的实验现象为___________________________________________________
________________________________________________________ _________。
_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
|
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在标号元素中,最活泼的金属元素是 。最活泼的非金属元素是 。
⑨元素的离子结构示意图是 。
(2)①与②形成共价化合物的电子式 。用电子式表示⑤与⑨形成化合物的形成过程 。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是 。
(4)⑦、⑧、⑨元素所形成的气态氢化物中,最稳定的是 。
⑦、⑧、⑨三种元素的最高价含氧酸的酸性由强到弱的顺序 。
(5)写出⑥元素的单质与盐酸反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时有关弱酸的电离平衡常数:( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.amol·L—1HCN溶液与amol·L—1NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+),c(Na+)>c(CN-)
C.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO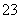 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的用途正确的是
可以用Na2O2漂白食品,而不能用SO2于干果防腐
B.用石英制太阳能电池
C. 食醋可去除水垢,NH4Cl溶液可去除铁锈
D.用电解熔融氯化铝的方法制得单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。
S2O32-和Cl2反应的产物之一为SO42-。下列说法不正确的
A.上述反应中,每生成l mol SO42-,可脱去1 mol Cl2
B.H2O参与该反应,既不做氧化剂又不做还原剂
C.根据该反应可判断氧化性:Cl2 > SO42-
D.该反应中还原剂是S2O32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述与对应图像或数据描述正确的是
A.由下列短周期元素性质的数据推断③元素最高价氧化物对应的水化物碱
性最强
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径最高或最低化合价 | 0.74 | 1.60 +2 | 1.52 +1 | 1.10 +5 | 0.99 +7 | 1.86 +1 | 0.75 +5 | 0.82 +3 |
| —2 | —3 | —1 | —3 |
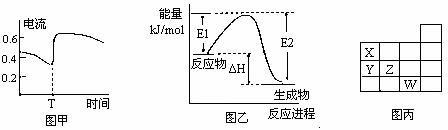
B.图甲表示Zn—Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2
C.图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变
D.图丙表示周期表的一部分,元素X,Y,Z、W中X的氢化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
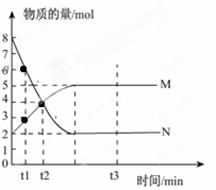
Ⅰ、一定温度下,在容积为V L的密闭容器中进行反应:aN(g)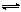 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
 (1)此反应的化学方程式中
(1)此反应的化学方程式中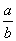 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)平衡时,N的转化率为 。
(4)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
II、某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:
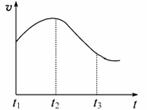
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
(1)试分析实验①中t1~t2速率变化的主要原因是 ,t2~t3速率变化的主要原因是 。
(2)实验②放出氢气的量减少的原因是 。
(3)某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?
(填“正确”或“不正确”)。请选择下列相应的a或b作答。
a、若不正确,请说明原因:
b、若正确则写出实验③中原电池的正极电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com