
| 事实 | 原因 | |
| A | 稀有气体的晶体属于原子晶体 | 其组成微粒是原子 |
| B | 键的极性H-O>H-S | 氧的电负性强于S的电负性 |
| C | HF稳定性比HI强 | HF分子间能形成氢键而HI不能 |
| D | 金刚石的熔沸点高于晶体硅 | C-C键能大于Si-Si键能 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、稀有气体的晶体属于分子晶体,原因分子间只存分子间作用力;
B、氧的电负性强于S的电负性,所以键的极性H-O>H-S;
C、氢化物的稳定性与中心元素的非金属性有关,而与氢键无关;
D、原子晶体的熔点高低与共价键的键能大小有关.
解答 解:A、稀有气体的晶体属于分子晶体,原因分子间只存分子间作用力,而不是原子晶体,故A错误;
B、氧的电负性强于S的电负性,所以键的极性H-O>H-S,故B正确;
C、氢化物的稳定性与中心元素的非金属性有关,F的非金属性强于碘的非金属性,所以HF稳定性比HI强,而与氢键无关,故C错误;
D、原子晶体的熔点高低与共价键的键能大小有关,C-C键能大于Si-Si键能,所以金刚石的熔沸点高于晶体硅,故D正确;
故选AC.
点评 本题考查了晶体类型、构成微粒等知识点,难度不大,注意稀有气体都是单原子分子,稀有气体中不存在化学键,只存在分子间作用力.


科目:高中化学 来源: 题型:填空题
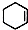 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
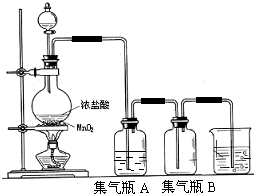
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY3一定是离子化合物 | |
| B. | 若Y的原子序数为m,则X的原子序数一定为m±4 | |
| C. | X和Y可属于同一周期,也可属于不同周期 | |
| D. | X和Y一定不属于同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O.lmol过氧化钠中,阴阳离子总数为0.4 NA | |
| B. | 11.2L氯气通入足量的NaOH充分反应,转移的电子数目为0.5 NA | |
| C. | 17g NH3气体含σ键的数目为3NA | |
| D. | 1L O.lmol/L氨水中,OH-数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③④ | C. | ②⑤⑥ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 煤经过干馏等物理变化可以转化为清洁燃料 | |
| C. | 煎炸食物的花生油和牛油都属于酯类,属于高分子化合物 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
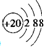 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.45 g | B. | 0.54 g | C. | 0.5 g | D. | 0.35 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com