
| A、H-是很强的氧化剂 |
| B、NH3具有还原性 |
| C、该反应的还原产物和氧化产物都是H2 |
| D、该反应属于置换反应 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
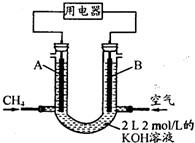 海底蕴藏着大量的“可燃冰”.用甲烷制水煤气(CO、H2),再合成甲醇来代替日益供应紧张的燃油.
海底蕴藏着大量的“可燃冰”.用甲烷制水煤气(CO、H2),再合成甲醇来代替日益供应紧张的燃油.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖 | B、甲酸乙酯 |
| C、丁醛 | D、甲醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| B、标准状况下,14g氮气含有的核外电子数为5NA |
| C、足量Zn与一定量的浓硫酸反应,产生标准状况下22.4L气体,转移的电子数为2NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com